CARBOXYLIQUES ACIDES
Parmi les acides organiques, caractérisés par la propriété de former un sel avec la soude ou la potasse, les acides carboxyliques, définis par le groupement carboxyle fonctionnel —CO2H, tiennent une place prépondérante.
Le plus anciennement connu est l'acide acétique CH3CO2H (du latin acetum, « vinaigre »), qui prend naissance par oxydation enzymatique des solutions diluées d'alcool éthylique, du vin par exemple. Il a été longtemps préparé par pyrolyse du bois à l'abri de l'air : il se forme un mélange complexe appelé pyroligneux dont les principaux constituants de la partie liquide sont le méthanol et l'acide acétique.
Le premier représentant de la fonction, l'acide formique HCO2H, doit son nom à sa présence chez la fourmi rouge, dont on l'a tiré autrefois.
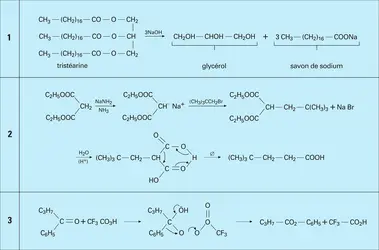
De très nombreux acides carboxyliques existent soit à l'état libre, soit le plus souvent à l'état d'esters, dans les produits naturels les plus divers : corps gras des huiles végétales et graisses animales, lipides des structures cellulaires, cytoplasmiques et membranaires. L'extraction des acides gras (à longue chaîne carbonée paire) des corps gras naturels est pratiquée de longue date par hydrolyse à chaud, ou saponification à la soude, suivie d'une acidification par l'acide sulfurique : le glycérol est facilement séparé des acides qui se solidifient au refroidissement. Les savons ou sels alcalins des acides gras étaient connus des Gaulois qui les utilisaient, semble-t-il, comme cosmétiques.
Nomenclature
La nomenclature officielle I.U.P.A.C. (International Union of Pure and Applied Chemistry) des acides carboxyliques est obtenue en remplaçant le e terminal de l'hydrocarbure correspondant par le suffixe -oïque et en faisant précéder le nom du terme acide : acide alcanoïque. Le numérotage est inutile, la fonction acide ne pouvant être portée que par un carbone primaire. Si l'acide est ramifié, on choisit comme chaîne principale la plus longue de celles qui portent la fonction. Lorsque cette nomenclature est compliquée, on désigne la fonction par le mot carboxylique utilisé comme suffixe : acide cyclohexanecarboxylique. Cependant, certains noms vulgaires, rappelant souvent l'origine de l'acide, restent en usage.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jacques METZGER : professeur de chimie organique à la faculté des sciences de Marseille
Classification
Pour citer cet article
Jacques METZGER. CARBOXYLIQUES ACIDES [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
ACÉTIQUE ACIDE
- Écrit par Jacques METZGER
- 2 111 mots
- 3 médias
L'acide acétique, acide organique de formule CH3COOH, est le membre le plus important de la famille des acides carboxyliques. Il joue avec ses dérivés un rôle essentiel dans de nombreuses synthèses et dégradations biologiques accompagnant le métabolisme des aliments et la formation des tissus....
-
ACÉTYLACÉTIQUE ESTER
- Écrit par Jacques METZGER
- 1 355 mots
- 2 médias
L'acide acétylacétique est le nom usuel du butanone-3-oïque :
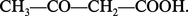
Cet acide a été isolé dans les urines pathologiques. Il peut être obtenu par une hydrolyse prudente de son ester éthylique. Ce dernier, beaucoup plus important, est un intermédiaire utilisé dans l'industrie pharmaceutique et dans...
-
ACIDES-ALCOOLS
- Écrit par Jacques METZGER
- 1 300 mots
- 1 média
Un acide-alcool est une molécule renfermant au moins une fonction acide carboxylique et une fonction alcool.
La nature nous en fournit de nombreux exemples : acides lactique du lait aigri, malique des pommes avant maturité (diacide-monoalcool), tartrique du tartre des vins (diacide-diacool), citrique...
-
ACIDES & BASES
- Écrit par Yves GAUTIER, Pierre SOUCHAY
- 12 364 mots
- 7 médias
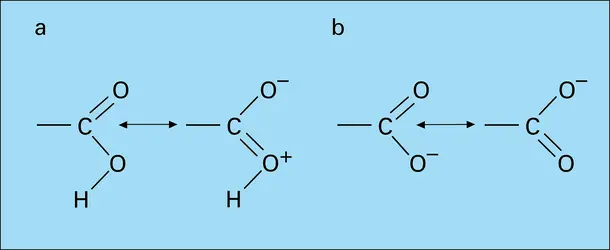
Un acide carboxylique s'ionise en un anion mésomère (formule 2), si bien qu'en fait la charge négative est répartie entre les deux atomes d'oxygène, donnant une structure intermédiaire entre les précédentes (on dit qu'il y a résonance entre celles-ci). La structure réelle... - Afficher les 15 références
Voir aussi
- HYDROLYSE
- PEROXYDES
- PERKIN RÉACTION DE
- CARBONÉE CHAÎNE
- SOLUBILITÉ
- CHIMIQUES INDUSTRIES
- HÉTÉROLYSE
- PROPIONIQUE ACIDE
- OXYDATION
- AMPHIPHILE MOLÉCULE
- DÉSHYDRATATION
- GRAS ACIDES
- NUCLÉOPHILES SUBSTITUTIONS
- DÉCARBOXYLATION
- KOLBE RÉACTION DE
- ANHYDRIDES D'ACIDES CARBOXYLIQUES
- ANHYDRIDE ACÉTIQUE
- ANHYDRIDE PHTALIQUE
- ALCOOLYSE
- ÉLECTRONIQUE STRUCTURE
- CONJUGAISON, chimie
- NOMENCLATURE, chimie
- HALOGÉNURES