NEUROVÉGÉTATIF SYSTÈME
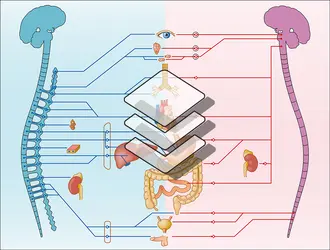
Le système neurovégétatif de l'homme, appelé également système « autonome, viscéral ou involontaire », se définit par son rôle et par son organisation anatomo-physiologique. Ses prolongements périphériques sont distribués à tous les organes et tissus situés à l'intérieur du corps ; il innerve les viscères (cœur, vaisseaux, tube digestif, etc.), leurs muscles et les glandes. Il joue un rôle de régulation et de coordination des fonctions dites végétatives, et intervient dans la plupart des activités métaboliques. Le résultat ultime de toute l'activité du système nerveux végétatif est « le maintien de la constance du milieu intérieur » (Claude Bernard, 1878), ou encore de « l'homéostasie de l'organisme » (Cannon, 1929). Il commande aux phénomènes végétatifs qui accompagnent tout comportement, qu'il s'agisse des adaptations végétatives (cardiovasculaires, respiratoires, etc.) qui sont nécessaires à toute dépense motrice, ou des signes visibles (vasodilatation cutanée, sudation, etc.) des comportements dits « affectifs » ; enfin, il sollicite le système nerveux commandant la vie de relation lorsque les régulations végétatives sont débordées (disparition de certaines réserves, accumulation de déchets) pour mettre en jeu des comportements liés aux « besoins primaires » (recherche et ingestion d'aliments, d'eau, de sels ; fonctions excrémentielles ; recherche du partenaire sexuel).
Le système nerveux végétatif (S.N.V.) se différencie ainsi, par son rôle, de l'autre grande subdivision du système nerveux, le système somatique, encore appelé système de la vie de relation ou système cérébro-spinal, qui comprend essentiellement les systèmes de la sensibilité, les systèmes de la motricité squelettique et les centres nerveux qui intègrent la sensorimotricité. Il s'en différencie également du point de vue de l'organisation anatomo-physiologique : on étudiera cette organisation au niveau périphérique et à celui des différents étages du système nerveux central ; le centre végétatif de commande le plus important est l'hypothalamus ; ses relations neurovasculaires avec l'hypophyse en font le point de départ des régulations de toutes les réactions neuro-endocriniennes. Les mécanismes de transmission au niveau des relais variés du S.N.V. utilisent soit des « neurotransmetteurs chimiques » (acétylcholine, noradrénaline), soit des « neurohormones » (hormones de libération hypothalamo-hypophysaires) ; les études biochimiques de la transmission ont été beaucoup plus faciles et précoces dans le cas du S.N.V. que dans celui du système somatique.
On exposera ici de façon analytique l'organisation anatomo-chimique de la périphérie, des centres de commande et des afférences végétatives. Un second chapitre indiquera les lois de fonctionnement du S.N.V. et ses rapports avec le système de la vie de relation.
Les systèmes effecteurs périphériques
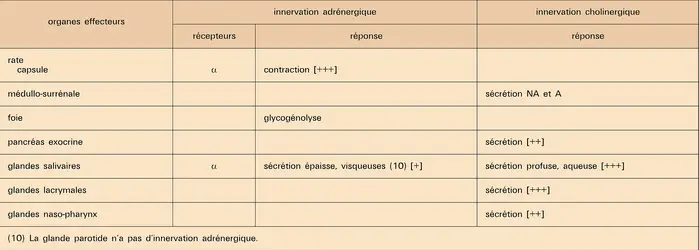
Deux systèmes distincts, le système orthosympathique (O.S.) et le système parasympathique (P.S.), caractérisés par leur organisation anatomique et la nature des neurotransmetteurs décelés au niveau des relais synaptiques, innervent les viscères et les glandes. On étudiera leur disposition anatomique puis leurs caractéristiques biochimiques.
Disposition anatomique
Système orthosympathique
Organisation au niveau d'un métamère
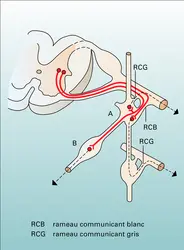
L'effecteur orthosympathique est constitué par deux neurones successifs : un premier neurone préganglionnaire myélinisé continué par un second neurone postganglionnaire amyélinisé. Ils s'articulent au niveau d'un ganglion situé en dehors de la moelle.
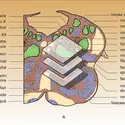
Les corps cellulaires (péricaryon) des neurones préganglionnaires sont situés dans la zone grise intermédio-latérale de la moelle. Leur axone se termine et s'articule avec le péricaryon du neurone[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Paul DELL : ancien directeur de recherche au C.N.R.S., Institut de neurophysiologie et de psychophysiologie, Marseille
Classification
Pour citer cet article
Paul DELL. NEUROVÉGÉTATIF SYSTÈME [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
BULBE RACHIDIEN
- Écrit par Paul LAGET
- 4 096 mots
- 5 médias
Ilest connu que le bulbe rachidien constitue une région d'importance vitale et que sa destruction ou une lésion même légère sont fatales (nœud vital de Flourens). Cela tient à la présence, au sein de la réticulée bulbaire, de centres de première importance pour le contrôle et la régulation respiratoire... -
CERVEAU HUMAIN
- Écrit par André BOURGUIGNON, Cyrille KOUPERNIK, Pierre-Marie LLEDO, Bernard MAZOYER, Jean-Didier VINCENT
- 12 782 mots
- 9 médias
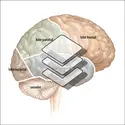
Sous le thalamus se trouve l'hypothalamus qui rassemble toutes les régulations viscérales participant à l'homéostasie du milieu intérieur. Véritable centrale végétative, il joue un rôle fondamental dans l'intégration des fonctions somatiques, autonomes et endocriniennes car il reçoit des informations... -
COMA
- Écrit par Marie-Elisabeth FAYMONVILLE, Geneviève LABORIT, Henri LABORIT, Steven LAUREYS, Pierre MAQUET
- 3 197 mots
- 3 médias
...artérielle, favoriser secondairement la défaillance circulatoire, ou collapsus, et l'élévation thermique. Dans cette forme de coma, la réactivité aux stimuli se traduit par des réponsesneurovégétatives (bouffées vasomotrices, troubles respiratoires et cardio-vasculaires, dilatation pupillaire). -
HOMÉOSTASIE
- Écrit par Jack BAILLET
- 4 842 mots
- 2 médias
De la même manière, les divers étages du système nerveux végétatif sont coiffés par un système diencéphalo- limbique dont l'activité apparaît de manière évidente après ablation du manteau cortical (Goltz, W. B. Cannon), ou par excitation directe de certaines zones (J. P. Karplus et A. Kreidl ; W. R.... - Afficher les 7 références
Voir aussi
- NERF PNEUMOGASTRIQUE ou NERF VAGUE
- POUMON
- TYROSINE
- ADRÉNERGIQUE SYSTÈME
- RELEASING FACTORS (RF)
- FSH (Follicle Stimulating Hormone) ou HORMONE FOLLICULO-STIMULANTE
- VASOPRESSINE ou HORMONE ANTIDIURÉTIQUE (ADH) ou PITRESSINE
- MÉDULLOSURRÉNALE
- MAO (monoamine oxydase)
- TEGMENTUM, neuroanatomie
- PRESSION SANGUINE
- HYDRIQUE ÉQUILIBRE
- CHÉMORÉCEPTEUR
- FAIM, psychophysiologie
- PHYSIOLOGIE
- DIABÈTE INSIPIDE
- NERFS CRÂNIENS
- BARORÉCEPTEUR
- NEUROPHYSIOLOGIE
- ORTHOSYMPATHIQUE SYSTÈME ou SYSTÈME NERVEUX SYMPATHIQUE
- PARASYMPATHIQUE SYSTÈME NERVEUX
- IMAO (inhibiteur de la monoamine oxydase)
- RÉGULATION BIOLOGIQUE
- NEURONES NORADRÉNERGIQUES
- RÉCEPTEUR, physiologie
- SATIÉTÉ, physiologie
- NEURONE ou CELLULE NERVEUSE
- NICOTINE
- OSMORÉCEPTEURS
- CHOLINESTÉRASES
- CHOLINERGIQUE SYSTÈME
- HYPERPHAGIE
- VÉGÉTATIVE VIE
- FEEDBACK ou RÉTROACTION
- NORADRÉNALINE
- RESPIRATION
- NEUROBIOLOGIE
- NEUROMÉDIATEURS ou NEUROTRANSMETTEURS
- NEUROENDOCRINOLOGIE
- ALIMENTAIRE COMPORTEMENT
- ALPHA-ADRÉNERGIQUES RÉCEPTEURS
- EFFÉRENCES, neurologie
- AFFÉRENCES, neurologie
- BÊTA-ADRÉNERGIQUES RÉCEPTEURS
- CIRCULATION SANGUINE
- NEUROTRANSMISSION
- NEUROLOGIE HISTOIRE DE LA
- PRISE ALIMENTAIRE
- ACÉTYLCHOLINESTÉRASE