ATOME
Atome et théorie du solide
La théorie atomique et les méthodes de la mécanique quantique ont permis une description détaillée des propriétés de la matière à l'état solide.
Les cristaux sont caractérisés par un arrangement très ordonné de leurs atomes tel qu'un réseau géométrique caractéristique se répète dans tout le cristal.
Les corps amorphes (les verres par exemple) sont constitués d'atomes qui ne sont que localement ordonnés. Un réseau d'atomes se prolonge dans un autre réseau un peu différent du premier.
Les principaux solides cristallins se classent, en général, dans les types suivants :
1. Les métaux et alliages métalliques ; les forces d'interaction responsables du maintien des atomes dans les réseaux métalliques sont nommées forces de liaison métallique. Les atomes dans le métal ont un électron qui n'est pas très fortement lié ; il en résulte que celui-ci peut migrer aisément d'un atome à l'autre, ce qui explique les propriétés de conductions électrique et thermique des métaux. Le gaz que formeraient de tels électrons obéit au principe de Pauli ; il est décrit par une théorie statistique due à Fermi et Dirac.
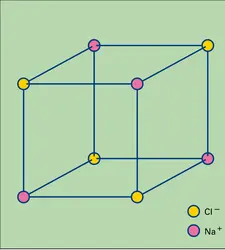
2. Les cristaux ioniques : les nœuds du réseau sont occupés par des ions.
3. Les cristaux moléculaires incluent des atomes ou molécules neutres dans leurs réseaux. Les forces de liaison entre ces atomes ou molécules sont les forces d'attraction de Van der Waals.
4. Les cristaux de valence sont constitués d'atomes dont les interactions sont des forces de liaison chimique (diamant) ; le couplage correspondant des électrons explique la grande résistance électrique de ces cristaux.
5. Les semi-conducteurs dont les propriétés résultent, en général, de la libération d'électrons par des impuretés insérées dans un réseau cristallin, avec mise en œuvre d'une énergie faible par rapport à l'énergie d'excitation d'un atome libre, énergie qui n'est pas très grande non plus en comparaison avec l'énergie thermique kT.
6. Les cristaux à liaison hydrogène, pour lesquels la cohésion est créée par le déplacement d'atomes d'hydrogène d'un radical vers la partie négative d'une autre molécule.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- José LEITE LOPES : professeur de physique nucléaire, université Louis-Pasteur, directeur du groupe physique théorique et hautes énergies du Centre de recherche nucléaire de Strasbourg
Classification
Pour citer cet article
José LEITE LOPES. ATOME [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
DESCRIPTION DE L'ATOME
- Écrit par Bernard PIRE
- 104 mots
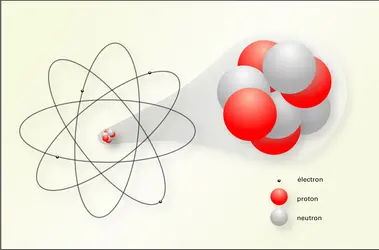
Ernest Rutherford (1871-1937) propose en 1911 un modèle planétaire de l'atome. L'interprétation des résultats expérimentaux obtenus par ses collaborateurs Hans Geiger et Ernest Marsden sur la déviation violente des rayons α une mince feuille d'or lui permet de comprendre qu'un atome est...
-
PARTICULES ÉLÉMENTAIRES
- Écrit par Maurice JACOB, Bernard PIRE
- 8 172 mots
- 12 médias
-
AGRÉGATS, physico-chimie
- Écrit par Jean FARGES, Rémi JULLIEN
- 1 616 mots
- 7 médias
...nombreuses méthodes physiques utilisées, la spectrométrie de masse est la plus importante. Elle permet en effet de classer les agrégats selon le nombre N d'atomes ou de molécules qu'ils contiennent. Ainsi, les spectres de masses, pour certaines valeurs de N appelées « nombres magiques », font apparaître... -
ALLIAGES
- Écrit par Jean-Claude GACHON
- 7 362 mots
- 5 médias
La seconde voie non expérimentale est celle de la théorie physique de l'état solide.Les atomes interagissent entre eux par l'intermédiaire de leurs couches électroniques externes, lesquelles sont bien décrites par la mécanique quantique. Des modèles des alliages ont été construits pour essayer,... -
BOHR ATOME DE
- Écrit par Bernard PIRE
- 369 mots
- 1 média
Deux ans après avoir soutenu sa thèse sur la théorie électronique des métaux, le physicien danois Niels Bohr (1885-1962) écrit en 1913 trois articles fondamentaux qui révolutionnent la compréhension de la structure de la matière. Le premier, paru le 5 avril dans le Philosophical Magazine...
- Afficher les 87 références
Voir aussi
- FRÉQUENCE, physique
- ONDE ou RAYONNEMENT ÉLECTROMAGNÉTIQUE
- ABSORPTION, physique
- ISOTOPES
- POSITONIUM ou POSITRONIUM
- ORBITALES ATOMIQUES
- NOYAU ATOMIQUE
- INTERACTIONS MOLÉCULAIRES
- ÉMISSION, physique
- HAMILTONIEN
- SCHRÖDINGER ÉQUATION DE
- CRISTAL IONIQUE
- AVOGADRO LOI D'
- GAY-LUSSAC LOI DE
- SCIENCES HISTOIRE DES, XIXe s.
- MÉCANIQUE ONDULATOIRE
- MUONS
- EXCITATION, physique
- CHARGE ÉLECTRIQUE
- QUANTIQUES NOMBRES
- TRANSITION, physique
- COVALENTE LIAISON
- FONCTION D'ONDE
- COUCHES ÉLECTRONIQUES
- ÉNERGIE POTENTIELLE
- SCIENCES HISTOIRE DES, Antiquité et Moyen Âge
- BREMSSTRAHLUNG ou RAYONNEMENT DE FREINAGE
- ÉMISSION SPONTANÉE
- ÉMISSION STIMULÉE ou ÉMISSION INDUITE
- HÉLIUM
- ÉLÉMENTS CHIMIQUES
- PROPORTIONS LOI DES, chimie
- QUANTIQUE MÉCANIQUE
- PAULI PRINCIPE D'EXCLUSION DE
- POSITONS ou POSITRONS
- SOLIDES PHYSIQUE DES
- HEISENBERG RELATIONS DE ou RELATIONS D'INCERTITUDE
- COMMUTATION RELATION DE
- RÈGLES DE SÉLECTION, physique
- ÉLECTRONIQUE STRUCTURE
- FRANCK & HERTZ EXPÉRIENCE DE
- RYDBERG FORMULE DE
- PROBABILITÉ DE TRANSITION
- PÉRIODIQUE CLASSIFICATION
- NIVEAU, physique atomique
- CONFIGURATION ÉLECTRONIQUE
- MUONIUM
- ATOME ARTIFICIEL
- CHIMIE HISTOIRE DE LA
- ATOME EXOTIQUE
- HÉLIUM MUONIQUE
- SPECTRE, optique
- MOMENT CINÉTIQUE ou MOMENT ANGULAIRE
- AVOGADRO NOMBRE D'
- RYDBERG CONSTANTE DE
- RAIE SPECTRALE
- RUTHERFORD ATOME DE
- DUALITÉ ONDE-CORPUSCULE
- LENNARD-JONES POTENTIEL DE
- PHYSIQUE HISTOIRE DE LA
- SCIENCES HISTOIRE DES
- ÉTAT QUANTIQUE