OXYGÈNE
Principales utilisations du dioxygène
Même au laboratoire, on ne s'adresse plus guère, pour la préparation du dioxygène, aux méthodes fondées sur la décomposition du chlorate ou du permanganate de potassium, de l'oxylithe (Na2O2, K2O4), etc. À partir de la distillation fractionnée de l'air, l'industrie fournit un gaz de qualité courante (99,5 p. 100) ou ultra pure (99,998 p. 100) contenant moins de 20 volumes d'impuretés par million. Le dioxygène est livré en bouteilles d'acier, à ogive blanche pour la France, contenant 10 Nm3 (m3 normaux) de gaz comprimé à 200 bars. Pour des quantités plus importantes, on transporte le dioxygène sous forme liquide dans des récipients isolants, et on emploie des évaporateurs fixes de grande capacité installés sur les lieux d'utilisation. Pour des centres de consommation élevée, la distribution se fait par canalisations (oxyducs). La carte ci-jointe représente les gazoducs installés dans le nord de l'Europe occidentale.
Dans un grand nombre de cas, pour les réactions d'oxydation en phase gazeuse ou les combustions (foyers domestiques et industriels), on n'emploie pas le dioxygène pur mais directement l'air atmosphérique.
La combustion à haute température
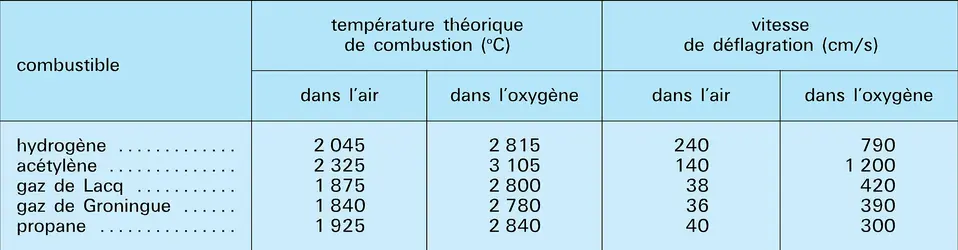
La présence du ballast de diazote dans les combustions avec l'air diminue considérablement l'enthalpie massique des produits de la combustion, donc la température des flammes et les vitesses de déflagration, ces deux paramètres influant directement sur la puissance de chauffe (tabl. 6). C'est la raison pour laquelle le chalumeau oxyacétylénique est un outil universellement utilisé pour le soudage, le brasage, la trempe superficielle, etc. Une des opérations les plus spectaculaires réside dans le coupage des métaux ; on se sert d'une buse spéciale comportant une injection centrale de dioxygène pur entourée d'une couronne de flammes oxyacétyléniques destinées à l'amorçage de la réaction qui, dans le cas des aciers, fournit un mélange d'oxydes fusibles (principalement Fe2O3). Cette technique permet de couper des épaisseurs atteignant un mètre et parfois plus dans certains cas. Elle est très employée dans les ateliers de chaudronnerie, dans les chantiers navals, etc. D'autre part, seules les combustions au dioxygène pur permettent de travailler le quartz, certains métaux nobles (Pt, Re) et les oxydes réfractaires (CaO, MgO, Al2O3). Des brûleurs oxycombustibles sont utilisés dans de nombreux fours industriels.
Le dioxygène en sidérurgie
L' affinage au dioxygène de la fonte a pratiquement bouleversé cette industrie. Deux méthodes sont utilisées : soufflage à l'aide d'une lance au-dessus du bain (procédés L.D. et Kaldo), ou barbotage par insufflation à la base du convertisseur (procédé O.B.M.). On tend même à utiliser le dioxygène en amont de l'élaboration de l'acier dans celle de la fonte ; on rajoute du dioxygène dans les vents des hauts fourneaux. De même le dioxygène est employé dans l'élaboration des aciers spéciaux à l'aide de fours électriques et dans celle des métaux non ferreux.
Le dioxygène dans l'industrie chimique
L' abaissement du prix de revient provenant de la fabrication en masse a permis d'utiliser le dioxygène dans plusieurs procédés de synthèse qui sont d'ailleurs en perpétuelle évolution suivant les impératifs économiques. On peut citer en chimie minérale : la synthèse de l'acide nitrique pur et concentré par oxydation de l'ammoniac (2 NH3 + 5/2 O2 → 2 NO + 3H2O ; NO + 1/2 O2 → NO2) ; la préparation de l'oxyde de titane par oxydation du chlorure TiCl4 ; la régénération du chlore par le procédé Deacon (2 HCl + 1/2 O2 → Cl2 + H2O) ; la délignification et le blanchiment de la pâte à papier par des mélanges (NaOH + O[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Robert CREUSE : chef du service information et gestion, direction des centres de recherche et de développement de la société Air liquide
- René NOTO : médecin-colonel, anesthésiste-réanimateur, chargé de l'enseignement de la médecine d'urgence et de la médecine de catastrophe au service de santé des armées
Classification
Pour citer cet article
Robert CREUSE et René NOTO. OXYGÈNE [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
AÉROBIOSE & ANAÉROBIOSE
- Écrit par Claude LIORET
- 2 734 mots
- 1 média
-
AÉRONOMIE
- Écrit par Gaston KOCKARTS
- 4 157 mots
- 11 médias
...reproductibles. De nouveaux constituants atmosphériques apparaissent et sont susceptibles d'influencer à leur tour la structure de l'atmosphère. En partant de l' oxygène moléculaire (O2), dont la première limite de dissociation est à 242,4 nm, le rayonnement solaire produit des atomes d'oxygène suivant le mécanisme... -
AIR
- Écrit par Jean PERROTEY
- 2 154 mots
- 2 médias
...vie. Le constituant actif est assimilé au gaz obtenu par calcination du salpêtre, ou « nitre », d'où le nom d'« esprit nitro-aérien » alors donné à l' oxygène. Un siècle plus tard, la nature de l'air est vraiment élucidée par Lavoisier. L'expérience par laquelle il établit la composition de l'air est,... -
ANÉMIES
- Écrit par Bruno VARET
- 3 091 mots
- 5 médias
...d'hémoglobine. Les constituants des globules rouges autres que l'hémoglobine semblent n'avoir pour fonction que de protéger l'hémoglobine de l'oxydation. La fonction essentielle de l'hémoglobine est le transport de l'oxygène. Il est donc logique que la baisse de la pression partielle en oxygène au niveau... - Afficher les 69 références
Voir aussi
- OZONE
- PEROXYDES
- ISOTOPES
- PARAMAGNÉTISME
- ÉPURATION DES EAUX
- RÉANIMATION
- RADIOÉLÉMENTS ou RADIONUCLÉIDES ou ISOTOPES RADIOACTIFS
- CAISSON HYPERBARE
- DÉPOLLUTION
- GAZODUC
- RESPIRATION ARTIFICIELLE ou VENTILATION ARTIFICIELLE
- CHIMIQUES INDUSTRIES
- OXYACÉTYLÉNIQUE CHALUMEAU
- DÉSINFECTANTS
- COVALENTE LIAISON
- MASSE ATOMIQUE
- EAU OXYGÉNÉE (peroxyde d'hydrogène)
- OZONIDES
- SUPEROXYDES
- ORBITALES MOLÉCULAIRES
- DOUBLE LIAISON ou LIAISON ÉTHYLÉNIQUE
- DEGRÉ D'OXYDATION
- OXYDATION
- OXYDANTS
- OXYGÈNE ATMOSPHÉRIQUE
- GAZEUX ÉTAT
- SINGULET ÉTAT
- ÉLECTRONIQUE STRUCTURE
- OXHYDRIQUE CHALUMEAU
- INSUFFISANCE RESPIRATOIRE
- CONFIGURATION ÉLECTRONIQUE
- SOINS INTENSIFS
- OXYGÉNOTHÉRAPIE
- RESPIRATOIRE PATHOLOGIE
- RESPIRATION
- RESPIRATION ASSISTÉE ou ASSISTANCE RESPIRATOIRE
- DÉTRESSE RESPIRATOIRE AIGUË
- OXYDES
- FLUORURES
- IONIQUE LIAISON
- VENTILATION PULMONAIRE
- URGENCES, médecine
- OXYGÈNE LIQUIDE