MATIÈRE (physique) États de la matière
D'Aristote à Réaumur, au xviiie siècle, la nature des solides ou des fluides a posé de grandes énigmes aux savants de jadis. Les découvertes de plus en plus fines de la science moderne sur l'organisation des molécules et des liaisons atomiques dans les matériaux ou dans les composés étudiés au laboratoire, comme dans les corps ordinaires de la vie quotidienne, expliquent largement l'origine de ces difficultés historiques ; elles obligent à revoir certaines divisions simplistes, issues à la fois des limites de l'expérience quotidienne et des orientations schématiques ou grossières de disciplines scientifiques naissantes.
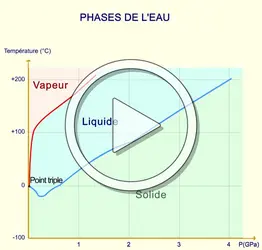
La division classique en états solide, liquide et gazeux est issue de la thermodynamique du xixe siècle. Elle dut subir une révision avec la découverte par les thermodynamiciens du xxe siècle de l'état critique, qui révélait une continuité de fait entre l'état gazeux et l'état liquide. On invoqua alors un état fluide, censé regrouper les états liquide, gazeux et critique, par opposition à l'état solide a priori mieux défini. Toutefois, dans la plupart des situations, la distinction entre liquide et gaz gardait tout son sens.
L'émergence dans le champ de la recherche des milieux extrêmement chauds obligea à introduire un quatrième état de la matière : l'état de gaz globalement neutre, mais constitué d'atomes ou de molécules ionisés, que l'on rencontre surtout en astrophysique (étoiles, ionosphères planétaires, aurores boréales, etc.) et dans un certain nombre de dispositifs industriels (ampoules au néon par exemple) ou militaires (bombe atomique). L'état ionisé se révélait si fondamentalement différent de l'état ordinaire de la matière qu'il méritait une nomenclature à part, le plasma. L'expression consacrée de « quatrième état de la matière » est équivoque : elle laisse entendre une proximité taxinomique du plasma avec l'état fluide ou l'état solide qui est davantage ancrée dans la traditionnelle nécessité d'une nomenclature que dans les faits scientifiques. Quand on décrit comme « état de la matière » l'état plasma, il faut être bien conscient que les concepts qui sous-tendent ce dernier sont presque sans rapport avec les attributs des états fluide et solide.
De son côté, la physique quantique a enregistré une série impressionnante de succès, dont le moindre ne fut pas la découverte des états supraconducteur et superfluide. Le superfluide quantique, lui aussi, fait éclater les catégories héritées d'une autre époque.
Mais à l'intérieur même des catégories habituelles fluide et solide, et sans aller jusqu'à invoquer des effets quantiques, des distinctions essentielles ont vu le jour, qui remettent en cause l'expérience quotidienne. En effet, le verre ordinaire, par exemple, quoique parfaitement solide au premier abord, se révèle posséder une structure bien plus proche de celle d'un liquide que de celle d'un quartz ou d'un grenat (cristaux typiques). À l'opposé, certains liquides sont constitués de molécules régulièrement ordonnées, ce sont les cristaux liquides. On parle parfois d'état mésomorphe pour ce type de corps, ce qui signifie état « intermédiaire » (entre liquide et solide). En découvrant, ou en inventant des corps nouveaux possédant, à l'état fluide, de nombreuses propriétés des solides ou, à l'inverse, des corps solides présentant la plupart des attributs des fluides, la science moderne a fait éclater les catégories recouvertes par les expressions état solide ou état fluide. À quel état rattacher une mayonnaise, une mousse, une peinture qui ne coule pas ? La physique des gels, celle des milieux dispersés, des argiles, des polymères ou des colles a permis de jeter une lumière sur des états de la matière qui,[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Vincent FLEURY : chargé de recherche au C.N.R.S., laboratoire de physique de la matière condensée, École polytechnique, Palaiseau
Classification
Pour citer cet article
Vincent FLEURY. MATIÈRE (physique) - États de la matière [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
ÉTAT DE LA MATIÈRE, notion d'
- Écrit par Bernard PIRE
- 1 521 mots
L'expérience quotidienne permet à chacun d'appréhender la notion d'état de la matière (parfois appelé phase) et celle de transition de phase qui lui est étroitement liée. L'exemple typique est celui des trois états si différents que prend l'eau lorsque sa température varie : à partir de 0 ...
-
MATIÈRE, notion de
- Écrit par Jean-Marc LÉVY-LEBLOND
- 2 022 mots
Le mot « matière » cache sous sa généralité abstraite une origine concrète fort éclairante. En latin archaïque, materia appartient à la langue rustique et désigne la substance dont est fait le tronc de l'arbre, en tant qu'elle est productrice (de branches, de feuilles). L'élargissement successif...
-
PARTICULES ÉLÉMENTAIRES
- Écrit par Maurice JACOB, Bernard PIRE
- 8 172 mots
- 12 médias
Les physiciens poursuivent l'étude de la structure de la matière dans le but de trouver plus d'unité et de simplicité dans un monde qui nous frappe par sa diversité et son apparente complexité. N'est-il pas remarquable de pouvoir ramener la variété quasi infinie des objets qui nous entourent...
-
ANTIMATIÈRE
- Écrit par Bernard PIRE, Jean-Marc RICHARD
- 6 931 mots
- 4 médias
...associé est bâti avec les antiquarks correspondants. Les mésons résultent de la liaison d'un quark et d'un antiquark. Dans cette description moderne, la matière est constituée par trois « générations » de quarks et de leptons, le nombre trois a été établi par les expériences du C.E.R.N. (laboratoire européen... -
ATOME
- Écrit par José LEITE LOPES
- 9 140 mots
- 13 médias
L'atome est le terme ultime de la division de la matière dans lequel les éléments chimiques conservent leur individualité. C'est la plus petite particule d'un élément qui existe à l'état libre ou combiné. On connaît 90 éléments naturels auxquels s'ajoutent le ...
-
BOHR ATOME DE
- Écrit par Bernard PIRE
- 369 mots
- 1 média
Deux ans après avoir soutenu sa thèse sur la théorie électronique des métaux, le physicien danois Niels Bohr (1885-1962) écrit en 1913 trois articles fondamentaux qui révolutionnent la compréhension de la structure de la matière. Le premier, paru le 5 avril dans le Philosophical Magazine...
- Afficher les 37 références
Voir aussi
- PRESSION, physique
- LIQUIDE ÉTAT
- ÉTATS DE LA MATIÈRE
- EAU, physico-chimie
- PHASE TRANSITIONS DE
- PHASES ESPACE DES
- DISPERSION, chimie
- ÉTAT CHANGEMENT D'
- POINT CRITIQUE
- DIAGRAMME, thermodynamique
- POINT TRIPLE, thermodynamique
- PLASMAS
- IONISÉS MILIEUX
- BOSONS
- THIXOTROPIE
- VAPEUR D'EAU
- PHASES RÈGLE DES ou RÈGLE DE GIBBS
- GAZEUX ÉTAT
- TEMPÉRATURE
- LIQUIDE-VAPEUR ÉQUILIBRE
- MINÉRAUX
- MÉTALLURGIE, histoire
- HÉLIUM 4
- SOLIDE ÉTAT
- VAPEUR, chimie physique
- PHYSIQUE HISTOIRE DE LA
- QUARTZ
- SCIENCES HISTOIRE DES
- ÉTAT QUANTIQUE