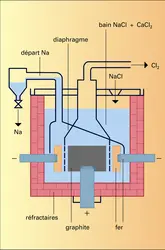
SODIUM
Bibliographie
M. Bernard, Cours de chimie minérale, Dunod, Paris, 1990
J. Besson, La Chimie minérale, coll. Que sais-je ?, P.U.F., Paris, 1976
A. Chrétien, R. Kohlmuller, P. Pascal & A. P. Rollet, « Sodium », in P. Pascal dir., Nouveau Traité de chimie minérale, t. II, fasc. I, Masson, Paris, 1966
A. Colas, Le Sel, coll. Que sais-je ?, P.U.F., 2e éd. 1993
O. J. Foust, Sodium-Na K Engineering Handbook, 4 vol., Gordon and Breach Science, New York, 1972-1979
G. Lucenet, « Le Sodium, un métal apprivoisé », in Revue française de l'électricité, no 279, Paris, 1983
R. Perrin & J. P. Scharff, Chimie industrielle, Masson, Paris, 1993
M. Salmon, « Sodium », in Techniques de l'ingénieur. Génie des procédés J4, Paris, 1990.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Luc AUFFRET : ingénieur, directeur du marketing de Métaux spéciaux S.A.
- Albert HÉROLD : professeur à l'Institut, université de Paris-I
- André METROT : docteur ès sciences, maître assistant à l'Institut national polytechnique de Nancy
- Bernard PIRE : directeur de recherche émérite au CNRS, centre de physique théorique de l'École polytechnique, Palaiseau
Classification
Pour citer cet article
Luc AUFFRET, Albert HÉROLD, André METROT et Bernard PIRE. SODIUM [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
BOROPHÈNE
- Écrit par Bernard PIRE
- 990 mots
- 1 média
...propriétés, et sans doute à de nombreux développements technologiques. Une première application possible du borophène pourrait concerner les piles à base de sodium. En effet, le développement de ces piles – qui bénéficieraient par rapport à celles au lithium du caractère abondant et bon marché de l’élément... -
GLUTAMATE DE SODIUM
- Écrit par Geneviève DI COSTANZO
- 163 mots
Sel monosodique monohydraté de l'acide L(+) glutamique. Il augmente la saveur de nombreux aliments, les hydrolysats protéiques entre autres. Cette propriété, découverte en 1908 par le Japonais Ikeda Kikunae (1864-1936), le fait employer depuis lors comme arôme, en particulier dans des préparations...
-
MÉTAUX - Métaux alcalins
- Écrit par Jean PERROTEY
- 3 023 mots
- 4 médias
-
NUCLÉAIRE - Réacteurs nucléaires
- Écrit par Jean BUSSAC, Frank CARRÉ, Robert DAUTRAY, Jules HOROWITZ, Jean TEILLAC
- 12 438 mots
- 9 médias
...) et l' hélium sous pression. Parmi les liquides, l' eau ordinaire et l' eau lourde, qui sont aussi des modérateurs, ont la faveur des réacteurs à neutrons thermiques. Les réacteurs à neutrons rapides, qui excluent l'emploi de noyaux légers, ont utilisé des métaux fondus tels que le sodium. - Afficher les 11 références
Voir aussi
- SOUDE (hydroxyde de sodium)
- CARBONATE DE SODIUM
- SULFURES
- SELS
- SEL MARIN
- EAU, physico-chimie
- TEMPÉRATURE DE FUSION
- FUSION
- FLUIDE CALOPORTEUR
- SELS MINÉRAUX
- HYDRURES
- CARBURES
- CHIMIQUES INDUSTRIES
- ALCALINS
- CHLORURE DE SODIUM
- OXYDATION
- SULFATE DE SODIUM
- RÉDUCTEUR, chimie
- LEBLANC PROCÉDÉ
- HALITE
- ÉCLAIRAGE
- PHOSPHATES
- SEL GEMME
- BOUVEAULT & BLANC RÉACTION DE
- BLANCHETTIÈRE MÉTHODE DE
- CYANURE DE SODIUM
- CASTNER PROCÉDÉ
- DOWNS PROCÉDÉ
- PLOMB TÉTRAÉTHYLE
- SOLVAY PROCÉDÉ
- OXYDE DE SODIUM
- BOROHYDRURES
- HALOGÉNURES
- NITRATES
- ÉLECTROLYSE