ANILINE
L' aniline est un composé organique renfermant une fonction amine primaire, c'est-à-dire un atome d'azote lié à un carbone et à deux hydrogènes ; l'atome de carbone appartenant à un noyau benzénique, il s'agit d'une amine aromatique, la plus simple de toutes. Elle a pour formule : C6H5NH2.
C'est un liquide incolore, brunissant sous l'action de l'air et de la lumière, à l'odeur très désagréable ; peu soluble dans l'eau (34 g/l à 20 0C), elle a une masse spécifique de 1,024 g/cm3 ; elle se solidifie à − 6 0C et bout à 184 0C. C'est un produit assez toxique, que ce soit par injection ou par contact avec la peau ; l'inhalation de fortes quantités de vapeur provoque des vertiges et un état d'agitation.
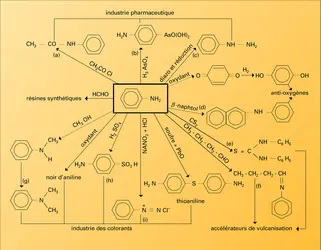
L'aniline est la matière de base de l'industrie des matières colorantes ; elle est très employée dans la synthèse des colorantsazoïques et c'est le point de départ de la fabrication de l'indigo. Elle est aussi utilisée dans l'industrie pharmaceutique et dans celle des matières plastiques, mais plus de la moitié de la production d'aniline est consommée en tant qu'accélérateur de la vulcanisation des caoutchoucs.
Propriétés chimiques
La conjugaison du doublet porté par l'azote avec le système aromatique a pour conséquence un affaiblissement de la basicité de la fonction amine par rapport au cas des amines aliphatiques et une activation des positions ortho- et para- du cycle vis-à-vis de la substitution électrophile. Le pKa de l'aniline est ainsi de 4,6 alors que celui de l'ammoniac est de 9,2 et celui de la méthylamine de 10,7. L'aniline donne cependant des sels avec les acides forts ; ces sels sont solubles dans l'eau avec une importante hydrolyse.
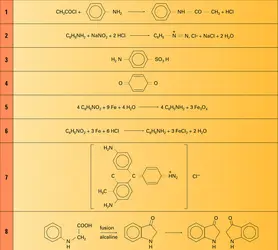
Les hydrogènes portés par l'azote sont mobiles, ce qui permet de les remplacer soit par des chaînes carbonées ouvertes, saturées ou non (réaction d'alcoylation), soit par des noyaux aromatiques (réaction d'arylation) ; le méthanol fournit ainsi la mono- et la diméthylaniline ; les phénols (C6H5OH) et les amines aromatiques conduisent à des amines secondaires. Les chlorures (R − COCl) et les anhydrides d'acides carboxyliques (R − CO − O − CO − R) permettent le remplacement d'un hydrogène porté par l'azote par un radical − CO − R (réaction d' acylation) ; il se forme des amides monosubstitués à l'azote par le noyau benzénique, appelés anilides ; ainsi le chlorure d'acétyle donne l'acétanilide (réaction).
Ces acylations permettent de protéger le groupement amine en vue d'autres réactions (bromation, nitration...).
Le nitrite de sodium, en milieu acide, donne avec l'aniline des sels de diazonium, ou sels de diazobenzène (réaction).
La mobilité des hydrogènes liés à l'azote permet également des condensations avec les aldéhydes aliphatiques ; il se forme des amines stables, les bases de Schiff :

Les substitutions sur le noyau aromatique sont orientées en positions ortho- et para-. L'acide sulfurique conduit à l'acide sulfanilique (formule 3).
Les condensations sur le noyau se font, pour des raisons stériques, presque exclusivement en position para-. L'aniline est susceptible de copuler avec les diazoïques pour donner des aminoazoïques qui sont des matières colorantes. Il est également possible de condenser l'aniline avec d'autres amines aromatiques ; en présence d'oxygène, la toluidine (mélange d'ortho- et para- aminotoluène) et l'aniline fournissent un colorant du groupe du triphénylméthane, la rosaniline (ou fuchsine).
L'aniline est un composé oxydable ; le bichromate de potassium donne la benzoquinone (formule 4), produit très employé en tannerie. Cependant les chlorates alcalins, en présence de sels de cuivre ou[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Alain TRINQUIER : agrégé de l'Université
Classification
Pour citer cet article
Alain TRINQUIER. ANILINE [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
AMINES
- Écrit par Jacques METZGER
- 3 232 mots
- 4 médias
Les amines aromatiques primaires, secondaires et tertiaires sont des dérivés de l'ammoniac dont un hydrogène au moins est remplacé par un reste aromatique. Le représentant le plus important de cette famille est l'aniline ou monoaminobenzène. -
COLORANTS
- Écrit par Daniel FUES
- 6 772 mots
- 4 médias
...Alors qu'il tentait de synthétiser la quinine, ce jeune chimiste anglais, assistant du professeur August Wilhelm von Hofmann, obtint, en oxydant de l' aniline impure avec du bichromate, un colorant mauve, soluble dans l'eau et l'alcool, avec lequel il fut possible de teindre la soie. Ce colorant, baptisé... -
HOFMANN AUGUST WILHELM VON (1818-1892)
- Écrit par Universalis
- 315 mots
Le chimiste allemand August Wilhelm von Hofmann est né le 8 avril 1818 à Giessen, en Allemagne. Ses recherches sur l'aniline et celles de sir William Henry Perkin contribuèrent à poser les bases de l'industrie des colorants d'aniline.
Hofmann étudia la chimie sous la direction de...
Voir aussi
- VULCANISATION
- SUBSTITUTION, chimie
- INDIGO
- CHIMIQUES INDUSTRIES
- CONDENSATION, chimie
- ACYLATION
- SCHIFF BASES DE
- BENZOQUINONE
- NITROBENZÈNE
- AMINES AROMATIQUES ou ARYLAMINES
- SULFANILIQUE ACIDE
- NOIR D'ANILINE
- UNVERDORBEN OTTO (1806-1873)
- PHARMACIE & INDUSTRIE PHARMACEUTIQUE
- RÉDUCTION, chimie
- DIAZOÏQUES COMPOSÉS