PAULING LINUS CARL (1901-1994)
La biologie moléculaire
Pauling fut incité à obliquer vers la biologie par Warren Weaver (1894-1978), de la Fondation Rockefeller, qui eut l'intuition des vastes possibilités offertes par les grands problèmes de la biologie, s'il parvenait à y intéresser des physiciens et des chimistes. Un petit nombre d'autres pionniers, comme John Desmond Bernal (1901-1971) en Angleterre, commençaient à étudier la structure des protéines au moyen de la diffraction des rayons X. Lors de son séjour en Europe, Pauling avait rencontré, en 1930 à Berlin, Hermann Mark (1895-1992), qui déjà faisait de même.
Pauling se lança lui aussi, hardiment car le sujet était d'une extrême difficulté, dans l'étude des protéines, avec Alfred Mirsky (1900-1974) de l'Institut Rockefeller. Les deux chercheurs différenciaient d'emblée les protéines fibreuses des protéines globulaires. Ils proposèrent d'interpréter ces dernières par un reploiement de la chaîne polypeptidique sur elle-même, une liaison hydrogène entre un groupement amino et l'atome d'oxygène d'un carbonyle en assurant le maintien. Ce faisant, ils affirmèrent la nature moléculaire, et macromoléculaire, des protéines, ce qui était loin d'être admis à l'époque.
Mais ce ne fut qu'au début des années 1950 que Pauling put enfin proposer des éléments de structure précis, les hélices α et les feuillets β responsables de la majeure partie de l'architecture protéique. Il le fit, dans une large mesure, à l'inspection de modèles moléculaires, dans lesquels les atomes sont représentés par des boules, reliées par des tiges. Son érudition structurale permit à Pauling de donner aux angles et aux longueurs de liaisons des valeurs raisonnables. On doit insister sur cet aspect. Constructeur de modèles moléculaires, grâce à la vaste banque de données structurales qu'il avait lui-même acquises, Pauling s'était constitué un outil aussi simple que puissant de prédiction de l'architecture atomique de nombreux édifices, celui des protéines en particulier. En 1953, Pauling, qui s'intéressait aussi à la structure de l'ADN, fut devancé sur le poteau par James Dewey Watson (né en 1928) et Francis Harry Compton Crick (1916-2004), qui bénéficièrent des splendides clichés cristallographiques qu'avait obtenus Rosalind Elsie Franklin (1920-1958), dans le laboratoire de Maurice Hugh Frederick Wilkins (1916-2004).

Linus Carl Pauling, 1955
Reproduced with permission of the Ava Helen and Linus Pauling Papers, Oregon State University Library
Le prix Nobel de chimie vint récompenser Pauling en 1954 pour son établissement des grands principes de l'architecture des protéines.
S'intéressant depuis des années (1935) à la molécule d'hémoglobine, Pauling, lorsqu'il entendit parler de l'anémie falciforme, pensa qu'il pouvait s'agir d'une « maladie moléculaire ». Cette affection, chez les porteurs homozygotes, est gravissime avec hémolyse, hypochromie et des globules rouges en forme de faucille, dans le sang veineux à faible pression d'oxygène. Les globules rouges récupèrent un aspect normal dans le sang artériel. Irving J. Sherman (né en 1916) démontra en 1940 que la désoxygénation induit le phénomène, rendu réversible par réoxygénation. La diffusion de la maladie s'explique car les hétérozygotes, qui ne présentent aucune anémie clinique, résistent bien au Plasmodium vecteur de la malaria, mieux que des sujets n'ayant pas cette tare. En 1949, Pauling suggéra que cette anémie était causée par une anomalie dans la molécule d'hémoglobine, conduisant à son agrégation dans sa conformation libre d'oxygène. Effectivement, en 1957, Vernon M. Ingram (1924-2006) montrait que dans les chaînes β de l'hémoglobine un résidu glutamate, de charge électrique négative, était remplacé par un résidu valine, neutre ; ce qui expliquait la précipitation de l'hémoglobine. Pauling découvrit de la sorte la toute première maladie[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Pierre LASZLO : professeur honoraire à l'École polytechnique et à l'université de Liège (Belgique)
Classification
Pour citer cet article
Pierre LASZLO. PAULING LINUS CARL (1901-1994) [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
PAULING ET LES PROTÉINES
- Écrit par Paul MAZLIAK
- 231 mots
- 1 média
Après avoir appliqué la mécanique quantique aux liaisons chimiques et défini les liaisons faibles, Linus Pauling (1901-1994) se consacra à l'étude des protéines. Il élabora, en 1951, la structure secondaire des protéines fibrillaires (kératine des cheveux, fibroïne de la soie, etc.), point de départ...
-
ABZYMES
- Écrit par Joël CHOPINEAU, Universalis, Alain FRIBOULET, Sabine PILLE, Daniel THOMAS
- 1 038 mots
Le concept d'anticorps catalytique, ou abzyme (contraction d’antibodyet enzyme), fut énoncé dès les années 1940 par Linus Pauling. S’appuyant sur le fait que la réaction chimique de transformation d'une molécule en une autre passe par un état de transition, qui représente...
-
ACIDES & BASES
- Écrit par Yves GAUTIER, Pierre SOUCHAY
- 12 364 mots
- 7 médias
En chimie minérale, la règle de Pauling, approximative mais utile, donne la force en fonction du nombre n d'oxygènes non unis à H :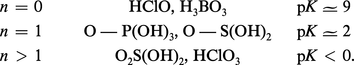
-
ANTIMOINE
- Écrit par Universalis, Jean PERROTEY
- 3 875 mots
- 3 médias
...), ce qui prouve que les atomes d'antimoine sont tous au même degré d'oxydation et non pas moitié de degré III et moitié de degré V. Pour expliquer ces faits, Linus Pauling a suggéré qu'il pourrait s'agir d'un cas de mésomérie, la formule réelle étant intermédiaire... -
CHIMIE THÉORIQUE
- Écrit par Lionel SALEM, François VOLATRON
- 4 288 mots
- 10 médias
...à ces deux structures. Chimiquement, cette construction est d'autant plus satisfaisante qu'elle s'accorde avec la notion de résonance introduite par Pauling, dans laquelle la molécule de benzène est supposée en quelque sorte alterner entre ces deux structures (ou en tout état de cause emprunter ses... - Afficher les 15 références
Voir aussi
- PACIFISME
- DRÉPANOCYTOSE ou ANÉMIE FALCIFORME
- STRUCTURE, biologie
- SCIENCES HISTOIRE DES, XXe et début du XXIe s.
- CHIMIE HISTOIRE DE LA
- QUANTIQUE CHIMIE
- MOLÉCULES BIOLOGIQUES, structure et fonction
- PROTÉINES
- ANTINUCLÉAIRES MOUVEMENTS
- BIOLOGIE HISTOIRE DE LA
- PHYLOGÉNIE MOLÉCULAIRE
- PRIX NOBEL DE CHIMIE
- PRIX NOBEL DE LA PAIX






