MÉTAUX Superplasticité des métaux
L'une des propriétés principales de l'état métallique est l'aptitude à la déformation sous l'effet d'une contrainte. Selon la valeur de celle-ci, la déformation résultante peut être élastique, c'est-à-dire qu'elle se résorbe si la contrainte cesse d'être appliquée, ou plastique, le solide conservant dans ce cas une déformation permanente après que la sollicitation mécanique a été supprimée. On caractérise quantitativement la plasticité par l'aptitude d'un métal ou d'un alliage donné à tolérer sans se rompre une déformation plus ou moins importante. Cette propriété, qui tient à la nature de la liaison entre atomes constituant le solide métallique, est spécifique : les solides non métalliques (verres, céramiques, cristaux ioniques, polymères...) présentent une cohésion qui dépend de liaisons fondamentalement différentes. Ce fait a pour conséquence soit que ces matériaux n'ont pratiquement pas de plasticité, soit qu'ils sont doués d'une plus ou moins grande capacité de déformation, mais que leur résistance mécanique intrinsèque reste limitée. Par contre, les solides métalliques témoignent généralement à la fois d'une notable résistance et d'une capacité importante de déformation.
Zones de déformation
Les modes de sollicitation mécanique sont fort nombreux : traction, compression, flexion, torsion, cisaillement... Le plus commun et le plus simple consiste à appliquer une force de tension uniaxiale (essai de traction) ; il peut donc être considéré à titre d'exemple pour définir les principales caractéristiques du comportement mécanique d'un matériau métallique. On supposera, pour rester dans le cas le plus général, que le matériau considéré est polycristallin, c'est-à-dire constitué de la juxtaposition de grains (chacun d'eux étant un monocristal plus ou moins parfait) séparés par des frontières appelées joints de grains. La courbe de traction classique obtenue à partir d'une éprouvette polycristalline est du type de celle qui est représentée sur la figure 1. Les paramètres portés sur le graphe sont, en ordonnées, l'effort F appliqué ou contrainte apparente (S0 désignant la section droite initiale de l'éprouvette) :


Il faut distinguer sur la courbe trois zones, qui sont représentées sur la figure 1.
Zone I
La portion correspondant à la zone I de la courbe de traction est un segment de droite OA. La déformation est donc élastique, homogène et réversible ; de plus, il y a proportionnalité entre les contraintes appliquées et les déformations élastiques résultantes. Le comportement élastique relève de la loi classique de Hooke :

E étant le module d'élasticité linéaire, ou module de Young, de valeur généralement élevée : les déformations élastiques sont donc faibles en valeur absolue.
L'ordonnée du point A définit la limite d'élasticité macroscopique σE ; la connaissance de cette valeur est fondamentale pour les calculs de résistance des matériaux. Lorsque le point A (ou limite de proportionnalité) est difficile à déterminer avec précision, on convient de mesurer ce que l'on appelle la limite d'élasticité macroscopique conventionnelle, soit la valeur de la contrainte entraînant une déformation permanente fixée arbitrairement (par exemple ε = 0,2 p. 100, d'où la valeur σE0,2).
Zone II
La portion correspondant à la zone II est un segment de courbe monotone AM à courbure non[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Georges CIZERON : professeur à l'université Paris-Sud, Orsay, directeur du laboratoire de structure des matériaux métalliques, Orsay
Classification
Pour citer cet article
Georges CIZERON. MÉTAUX - Superplasticité des métaux [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
ACIDES & BASES
- Écrit par Yves GAUTIER, Pierre SOUCHAY
- 12 364 mots
- 7 médias
Les métaux sont de même attaqués par les sels d'ammonium avec dégagement d'hydrogène :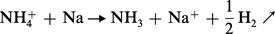
-
AGRÉGATS, physico-chimie
- Écrit par Jean FARGES, Rémi JULLIEN
- 1 616 mots
- 7 médias
Dans un agrégat métallique suffisamment petit, les électrons de conduction ne peuvent plus sauter d'un état quantique à l'autre car la différence d'énergie entre deux états successifs (qui varie comme 1/N) devient plus grande que l'énergie thermique. Par conséquent, lorsque la valence du métal considéré... -
ALLIAGES
- Écrit par Jean-Claude GACHON
- 7 362 mots
- 5 médias
Les alliages représentent une illustration matérielle du vieux dicton « l'union fait la force ». L'homme a toujours cherché des matériaux plus performants à l'utilisation, plus faciles à fabriquer ou à mettre en œuvre et plus économiques. Les alliages métalliques sont particulièrement...
-
ALUMINIUM
- Écrit par Robert GADEAU, Robert GUILLOT
- 9 636 mots
- 19 médias
Bien qu'il ne soit passé dans le domaine industriel qu'à la fin du xixe siècle, après la découverte par Paul Louis Toussaint Héroult et Charles Martin Hall du procédé de fabrication par électrolyse, l'aluminium est devenu le premier des métaux non ferreux. Sa légèreté, son inaltérabilité...
- Afficher les 94 références
Voir aussi
- MATÉRIAUX SCIENCE DES
- FLUAGE
- ÉCROUISSAGE
- DUCTILITÉ
- MÉCANIQUES FABRICATIONS
- HOOKE LOI DE
- EFFORTS, mécanique
- MACLES
- SOLIDE MÉCANIQUE DU
- LIMITE ÉLASTIQUE
- DÉFORMATIONS, mécanique
- CONTRAINTES, mécanique
- GLISSEMENT
- DÉFAUTS, cristallographie
- YOUNG MODULE DE ou MODULE D'ÉLASTICITÉ LONGITUDINALE
- TRACTION, science des matériaux
- STRICTION
- LACUNE, cristallographie
- MONOCRISTAUX
- CONSOLIDATION, mécanique
- FORMAGE
- SUPERPLASTICITÉ DES MÉTAUX
- TÔLE
- FAÇONNAGE
- TEMPÉRATURE
- TRÉFILAGE
- ALLONGEMENT, science des matériaux
- PLASTICITÉ
- RUPTURE, technologie
- ALLOTROPIE
- ESSAIS, matériaux
- JOINT DE GRAINS
- GRAIN, cristallographie









