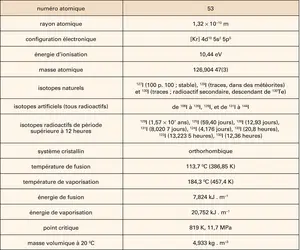
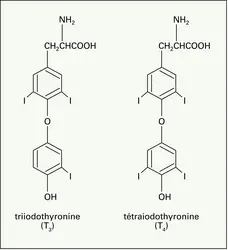
IODE
Effets relativistes
La chimie quantique calcule les propriétés moléculaires par résolution de l'équation de Schrödinger (cf. atome). Mais, lorsqu'il s'agit d'atomes lourds, des conséquences de la théorie de la relativité entrent en ligne de compte. Il convient dès lors de chercher des solutions à l'équation de Dirac (cf. antimatière) plutôt qu'à celle de Schrödinger. On sait que la masse d'une particule augmente avec la vitesse dont elle est animée, tendant vers une masse infinie à la vitesse de la lumière. Dans les atomes, les électrons internes sont animés des vitesses les plus grandes, qui peuvent atteindre 60 p. 100 de la vitesse de la lumière. D'où d'importants termes correctifs d'origine relativiste. Les conséquences observables sont multiples : alors que pour l'argent, la contribution relativiste est de peu d'importance, elle devient cruciale pour la chimie de l'or ; c'est pourquoi ce dernier diffère tellement de l'argent, tant par sa couleur jaune que par son inaltérabilité de métal noble. C'est aussi la raison pour laquelle le mercure est un liquide à température ambiante.
Dans le cas de l'iode, et des calculs quantiques sur les molécules comportant des atomes d'iode, ces effets relativistes sont eux aussi importants. Les molécules diatomiques ayant un atome d'iode ont des liaisons affaiblies par ces effets, plus longues et avec des énergies de dissociation moindres. Le moment dipolaire électrique en est accru de 10 à 20 p. 100.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Pierre LASZLO : professeur honoraire à l'École polytechnique et à l'université de Liège (Belgique)
Classification
Pour citer cet article
Pierre LASZLO. IODE [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
ALIMENTATION (Économie et politique alimentaires) - Malnutrition dans le monde
- Écrit par Laurence ROUDART
- 7 611 mots
- 9 médias
La carence en iode est également très répandue. À partir de certains seuils et selon les sujets, cette insuffisance cause la formation d'un goitre thyroïdien, une arriération mentale et des cas de surdité-mutité chez les nouveau-nés. -
ANTISEPSIE ET ASEPSIE
- Écrit par Gabriel GACHELIN
- 587 mots
- 1 média
Classiquement, l’histoire de la chirurgie est scandée par deux dates : l’année 1846, au cours de laquelle l’anesthésie à l’éther est utilisée pour la première fois ; l’année 1867, au cours de laquelle le chirurgien britannique Joseph Lister (1827-1912) décrit le succès d’une...
-
CATALYSE
- Écrit par Henri Jean-Marie DOU, Jean-Eugène GERMAIN
- 8 394 mots
- 7 médias
Ainsi, vers 600 0C, la vapeur d'iode s'empare de l'hydrogène des alcanes pour former de l'acide iodhydrique et des alcènes ou des hydrocarbures dérivés du benzène, de rapport H/C plus faible. D'autre part, l'oxygène attaque l'acide iodhydrique en lui arrachant son hydrogène, pour... -
HALOGÈNES
- Écrit par Jacques METZGER, Robert de PAPE
- 6 600 mots
- 5 médias
Les dérivés halogénés résultent du remplacement, par des halogènes F, Cl, Br, I, d'un ou de plusieurs atomes d'hydrogène des hydrocarbures. Ils se rencontrent rarement à l'état naturel : présence d'iode dans la tyroxine, présence de chlore dans l'antibiotique chloromycétine.... - Afficher les 12 références
Voir aussi
- THYROÏDIENNES HORMONES
- ISOTOPES
- RADIOÉLÉMENTS ou RADIONUCLÉIDES ou ISOTOPES RADIOACTIFS
- RADIOTHÉRAPIE
- ESSAIS NUCLÉAIRES
- TRACEURS RADIOACTIFS ou RADIOTRACEURS
- EAU DE MER
- TRIIODOTHYRONINE (T3)
- GOITRES
- COURTOIS BERNARD (1777-1838)
- DÉCHETS RADIOACTIFS ou DÉCHETS NUCLÉAIRES
- ISOTOPES, biologie
- NUCLÉAIRE POLLUTION