GÉNIE CHIMIQUE
Les bases scientifiques
Lois d'équilibre entre phases
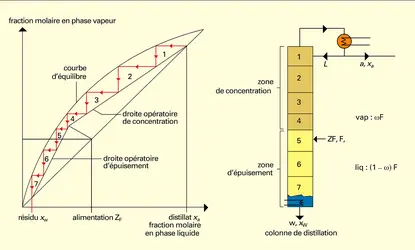
La connaissance des lois d'équilibre entre phases, par une analyse thermodynamique du système ou, tout simplement, par une série d'expériences, est fondamentale pour savoir si une séparation est possible ou non. L'examen des courbes d'équilibre permet d'apprécier a priori si l'opération unitaire envisagée sera plus ou moins difficile à réaliser.
Les lois d'équilibre entre phases sont tirées des principes de la thermodynamique des solutions, notamment par l'application du deuxième principe, en écrivant, pour les phases en présence, l'égalité des potentiels chimiques de chaque constituant (conditions d'un équilibre stable). Si nous considérons deux phases G et L et si nous explicitons chaque potentiel chimique en fonction d'un potentiel dit standard μi0, de la fraction molaire xi et d'un coefficient d'activité γi, nous pouvons écrire de manière générale :
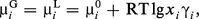
Les lois d'équilibre les plus simples qui sont accessibles par la théorie sont celles des solutions diluées. Entre un gaz et une vapeur, la pression partielle Pi d'un composé i en équilibre avec un liquide de fraction molaire xi et de tension de vapeur Pi0 s'écrit par exemple :
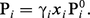
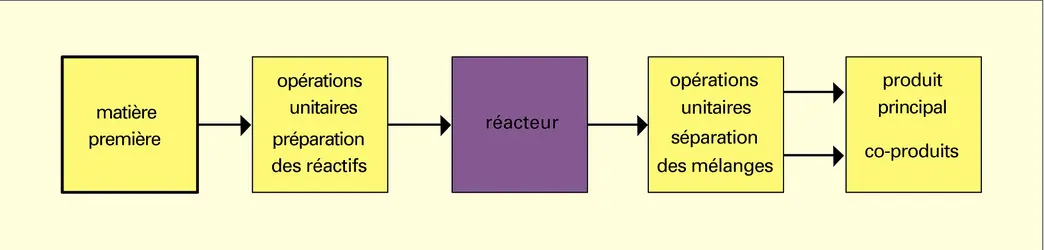
Analyse fonctionnelle des procédés
Le génie chimique s'intéresse principalement aux bilans matière et énergie fondés sur le premier principe de la thermodynamique :
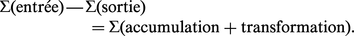
Cinétique de transfert
On distingue fondamentalement deux types de cinétique : la cinétique chimique, qui étudie les vitesses de transformation de la matière par voie réactionnelle, et la cinétique physique, qui concerne les transferts par diffusion (moléculaire ou turbulente).
Cinétique chimique
De manière très générale, la formation ou la disparition d'un composé par transformation chimique ou biochimique peut être décrite par un schéma réactionnel du type :
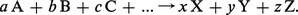
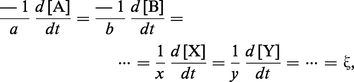
La vitesse de réaction (ici, production du composé X) s'exprime au moyen de l'équation générale :
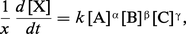
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Henri ANGELINO : directeur de l'École nationale supérieure d'ingénieurs de génie chimique, Toulouse
- Henri GIBERT : professeur à l'Institut national agronomique, Paris-Grignon, chef du département équipement des industries agro-alimentaires du Cemagref
- Pierre PIGANIOL : conseil en politique scientifique
Classification
Pour citer cet article
Henri ANGELINO, Henri GIBERT et Pierre PIGANIOL. GÉNIE CHIMIQUE [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
AMMONIAC
- Écrit par Henri GUÉRIN
- 5 033 mots
- 5 médias
La synthèse de l'ammoniac repose sur la réaction équilibrée :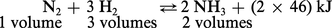
-
CENTRIFUGATION
- Écrit par Jean LEMERLE
- 1 797 mots
- 3 médias
Lorsque la décantation de particules sous l'effet du champ de pesanteur est inefficace ou trop lente, on a alors recours au procédé de centrifugation. Pour cela, on substitue au champ de pesanteur terrestre un champ de forces centrifuges infiniment plus grand, soit de 500 000 à 1 million de fois l'accélération...
-
CHIMIE - Histoire
- Écrit par Élisabeth GORDON, Jacques GUILLERME, Raymond MAUREL
- 11 186 mots
- 7 médias
Enfin, le génie chimique est une discipline indispensable pour le transfert des procédés de l'échelle du laboratoire à celle de l'industrie. Il a pour principale tâche d'optimiser les réactions par rapport aux données techniques, économiques et sociales et par rapport à l'environnement. -
CINÉTIQUE CHIMIQUE
- Écrit par Lucien SAJUS
- 9 646 mots
- 7 médias
...aussi une science appliquée ; en traduisant la transformation chimique en termes quantitatifs, elle rend possible l'action de l'ingénieur sur celle-ci. Un premier groupe d'application concerne la mise au point des procédés industriels de transformation chimique. Le problème dans ce cas est de fabriquer... - Afficher les 18 références
Voir aussi
- COMMANDE
- PLATEAU, génie chimique
- ÉTAGE, génie chimique
- SIMULATION
- ÉCOULEMENTS
- ÉQUILIBRE THERMODYNAMIQUE
- INGÉNIERIE
- VITESSE DE RÉACTION
- CHIMIQUES INDUSTRIES
- FICK LOI DE
- FOURIER LOI DE
- SÉPARATION, chimie
- THERMODYNAMIQUE CHIMIQUE
- RÉACTEUR CHIMIQUE
- THERMODYNAMIQUE PRINCIPES DE LA
- CONCENTRATION, chimie
- INSTALLATION PILOTE
- ÉNERGIE CONVERSION D'
- DISPERSÉS SYSTÈMES
- COLONNE, génie chimique
- CONTRÔLE, informatique et automatique
- ÉNERGIE THERMIQUE
- SOLUTION, chimie
- TECHNIQUES HISTOIRE DES, XXe et début du XXIe s.
- CONCEPTION ASSISTÉE PAR ORDINATEUR (CAO)
- PERFORMANCES, technologie
- PHASES, physico-chimie
- NEWTON LOIS DE, mécanique
- MODÉLISATION
- MODÈLE, chimie