VITESSE DE RÉACTION
Articles
-
CATALYSE
- Écrit par Henri Jean-Marie DOU et Jean-Eugène GERMAIN
- 8 394 mots
- 7 médias
Endeuxième lieu, puisque le catalyseur ne peut déplacer la position finale d'un équilibre chimique, mais qu'il diminue fortement le temps nécessaire pour l'atteindre, c'est qu'il accélère dans le même rapport les vitesses des deux réactions inverses dont l'égalité est la condition de l'équilibre. Ainsi,... -
CINÉTIQUE CHIMIQUE
- Écrit par Lucien SAJUS
- 9 646 mots
- 7 médias
...beaucoup plus facile si l'on est en présence d'une réaction chimique isolée, c'est-à-dire conduisant à un système unique de produits stœchiométriquement liés. Dans ce cas, en effet, les vitesses relatives aux réactifs ou aux produits seront proportionnelles entre elles et il suffira d'en étudier plus spécialement... -
COORDINATION (chimie) - Composés de coordination
- Écrit par Jean AMIEL et Jean-Pierre SCHARFF
- 4 894 mots
- 4 médias
...dans les complexes octaédriques d'un ion comme Co3+, par exemple, ont montré que l'étape importante (c'est-à-dire celle qui détermine la vitesse de la réaction) est celle qui implique la rupture de la liaison entre Co3+ et le groupe sortant. Le groupe entrant n'est pas impliqué dans cette... -
ENZYMES - Cinétique enzymatique
- Écrit par Christophe LÉGER
- 5 143 mots
- 8 médias
La loi de vitesse d'une réaction chimique est l'équation qui relie la vitesse de la réaction aux concentrations en réactifs et à des constantes de vitesse. Il arrive fréquemment que la vitesse suive ce qu'on appelle en mathématiques une loi de puissance : la vitesse est alors proportionnelle aux concentrations... -
ENZYMES - Site actif
- Écrit par Gabriel GACHELIN
- 3 957 mots
- 4 médias
...concentration en enzyme soit constante et qu'enfin l'environnement physico-chimique (solvant, tampon, ions cofacteurs, température, pH) soit constant, alors la vitesse v de production de P observée pour une concentration constante de S s'écrit comme v = Vps/(KM + s) où Vp est la vitesse maximale... -
GÉNIE CHIMIQUE
- Écrit par Henri ANGELINO , Henri GIBERT et Pierre PIGANIOL
- 7 794 mots
- 10 médias
La vitesse de réaction (ici, production du composé X) s'exprime au moyen de l'équation générale :où k désigne la constante de vitesse de réaction, qui dépend de la température selon la loi d'Arrhenius, et où α, β et γ sont les ordres de la réaction par rapport respectivement à A, B et...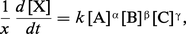
-
LIAISONS CHIMIQUES - Liaisons biochimiques faibles
- Écrit par Antoine DANCHIN
- 5 900 mots
- 9 médias
... et d'azote, ou encore des photons de la lumière visible). Comme tout catalyseur, une enzyme n'intervient dans la réaction que pour en accélérer la vitesse et sans être consommée au cours du processus d'activation. Ce qui est important, par conséquent, c'est la vitesse de rotation des... -
BRIGGS-HALDANE MODÈLE DE
- Écrit par Christophe LÉGER
- 526 mots
Les enzymes catalysent des réactions biochimiques dans des conditions physico-chimiques compatibles avec la vie. La cinétique de ces réactions, cinétique enzymatique, cherche à préciser les mécanismes par lesquels ces opérations sont réalisées, ou plus précisément déterminer les différentes constantes...
-
NUCLÉAIRE (PHYSIQUE) - Isotopes
- Écrit par René BIMBOT et René LÉTOLLE
- 5 400 mots
- 1 média
Des effets isotopiques beaucoup plus importants sont observés lorsque l'on considère les vitesses de réaction. L'interprétation exacte de ces phénomènes repose sur des considérations de mécanique statistique et, souvent, les mécanismes des réactions chimiques ne sont pas suffisamment bien connus pour... -
RÉACTION, chimie
- Écrit par Pierre LASZLO
- 2 707 mots
L' outil cinétique leur donna des éléments de réponse. Il continue d'être très utilisé. La vitesse d'une réaction se mesure par le taux de disparition, avec le temps, des partenaires réactionnels ou réactants, ou encore par le taux d'apparition, toujours avec le temps, des produits de cette réaction....

