ALCYNES
Propriétés chimiques
La réactivité des alcynes est caractérisée par l'importante insaturation du système acétylénique qui se traduit par des additions électrophiles, nucléophiles et radicalaires. Les alcynes vrais présentent une réactivité particulière du groupe Csp−H dont l'acidité est supérieure à celle de l'ammoniac.
Additions
Hydrogénation
L' hydrogénation des alcynes est facile et met en jeu les mêmes catalyseurs que pour les alcènes : le platine (Pt), le palladium (Pd) et le nickel (Ni). Sans précautions particulières, ce sont deux molécules d'hydrogène qui s'ajoutent en formant l'alcane. Cependant, la réaction de la première molécule d'hydrogène, conduisant à l'alcène, est plus exothermique que l'addition de la seconde sur ce dernier, de sorte qu'il est possible de réaliser l'hydrogénation partielle de l'alcyne en alcène en mettant en œuvre un catalyseur peu actif. Le palladium désactivé par des sels de métaux lourds et la quinoléine ou le fer de Raney permettent cette hydrogénation partielle qui conduit à peu près exclusivement à l'alcène cis (réaction 1a).
L'hydrogénation par voie chimique peut être réalisée par le sodium ou le lithium dans l'ammoniac liquide ou par l'hydrure de lithium et d'aluminium. Les alcènes étant insensibles à ces réactifs, cette méthode est sélective : elle conduit à l'alcène trans (réaction 1b).
Halogénation
Le chlore, le brome et l'iode se fixent sur les alcynes en donnant le dihalogénoéthylénique trans. La réaction est toutefois plus lente qu'avec les alcènes, comme le montre l'addition du brome sur le penten-4 yne-1 :
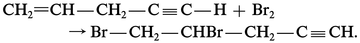
Hydrohalogénation
En l'absence de lumière et d'initiateurs radicalaires, les alcynes additionnent les acides chlorhydrique, bromhydrique et iodhydrique en formant un halogénure éthylénique qui peut, à son tour, se fixer à une seconde molécule d'hydracide. L'orientation de cette seconde addition est conforme à la règle de Markovnikov, et il se forme le dérivé gem-dihalogéné :
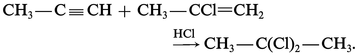
L'acétylène avec une molécule d'acide chlorhydrique conduit au chlorure de vinyle monomère, dont ce fut la première préparation industrielle (réaction 3).
L'acide fluorhydrique anhydre s'ajoute à l'acétylène pour donner le fluorure de vinyle puis le 1,1-difluoroéthane (réaction 4).
L'addition d'acide hypochloreux est facile, elle conduit aux dérivés carbonylés α-halogénés ; employé en excès, ce réactif donne les cétones α,α-dichlorées (réaction 5).
En présence de lumière et à basse température, la réaction de l'acide bromhydrique sur les alcynes suit un cours très différent : elle est radicalaire en chaîne, et le produit majoritaire résulte d'une addition cis, anti-Markovnikov (réactions 6) ; le radical organobromé intermédiaire est probablement attaqué par la molécule HBr sur sa face la moins encombrée.
Hydratation
En présence d'un acide fort et d'un sel mercurique catalyseur, les alcynes sont hydratés en énols qui se transforment en cétones (réaction 7). Dans le cas de l'acétylène, on obtient l'acétaldéhyde, dont ce fut un procédé industriel de fabrication.
Hydroboration
Selon un processus analogue à celui rencontré dans l'hydroboration des alcènes, le diborane B2H6 réagit avec les alcynes à 0 0C en formant un trivinylborane qui, comme dans le cas des alcènes,[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jacques METZGER : professeur de chimie organique à la faculté des sciences de Marseille
Classification
Pour citer cet article
Jacques METZGER. ALCYNES [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Article mis en ligne le et modifié le 14/03/2009
Médias
Autres références
-
ACÉTYLÈNE
- Écrit par Henri GUÉRIN
- 5 089 mots
- 6 médias
L'acétylène, de formule brute C2H2, est le premier terme des alcynes ou hydrocarbures acétyléniques de formule générale CnH2n-2. Ces derniers sont caractérisés par la présence d'une triple liaison (− C ≡ C−) dans leur molécule. L'acétylène présente une très grande...
-
ALCÈNES ou OLÉFINES
- Écrit par Jacques METZGER
- 3 640 mots
- 4 médias
L' hydrogénation ménagée des alcynes conduit aux alcènes : -
COORDINATION (chimie) - Chimie de coordination
- Écrit par René POILBLANC
- 3 996 mots
- 12 médias
Ilexiste de nombreux complexes dans lesquels un carbure acétylénique joue essentiellement le même rôle qu'un oléfine. Dans d'autres cas, l'existence de deux systèmes π dégénérés conduit l'alcyne, par duplication de la situation existant avec les oléfines, à se lier à deux atomes métalliques. C'est ce... -
ORGANOMÉTALLIQUES COMPOSÉS
- Écrit par Jacques METZGER et Charles PRÉVOST
- 4 208 mots
- 2 médias
Les organoplombiques se forment, en particulier, dans l'action du chlorure plombeux PbCl2 sur les organomagnésiens :






