HÉTÉROCYCLES
Les hétérocycles sont des composés chimiques dont la chaîne carbonée, cyclique, comporte un ou plusieurs atomes autres que le carbone ( hétéroatomes). Ils occupent une place chaque jour plus importante dans la chimie organique. Ces molécules réunissent en effet dans une même structure les caractères remarquables des composés cycliques saturés, partiellement saturés ou aromatiques, et ceux non moins intéressants des groupements fonctionnels construits autour des hétéroatomes.
Bien que dans certains cas (hétérocycles saturés en particulier) le comportement de ces molécules ne diffère pas sensiblement de celui de leurs analogues à chaîne ouverte, dans de très nombreux autres la cyclisation entraîne l'apparition de propriétés nouvelles, qui font de la plupart des molécules hétérocycliques les pièces uniques d'un ensemble original aux multiples applications.
Ces cycles peuplent abondamment les séries des composés naturels les plus divers, animaux ou végétaux, et la chimie des médicaments naturels ou de synthèse leur est redevable de ses plus belles réussites. Les mystérieuses propriétés des acides nucléiques en particulier sont directement liées à de subtiles différences de structure caractéristiques de quelques hétérocycles seulement. Peu d'industries fines peuvent se passer des hétérocycles, celle des colorants leur doit beaucoup, et la photographie en couleur n'existerait pas sans eux. L'industrie chimique plus lourde met à profit la très grande réactivité de certains d'entre eux, comme les époxydes, pour produire des matières intermédiaires, fondamentales pour l'économie moderne.
On conçoit que l'extrême diversité de ces composés rende difficile leur présentation dans un cadre logique, leur étude a cependant fait depuis le début du siècle suffisamment de progrès pour qu'une analyse systématique puisse être proposée sur la base de critères relativement simples.
Classification et nomenclature
Les hétérocycles sont habituellement classés selon le nombre de cycles et, pour chaque cycle, sa taille, son degré d'insaturation, le nombre et la nature des hétéroatomes.
Il est aisé de prévoir que le nombre des hétérocycles possibles est extrêmement grand, c'est pourquoi on se limitera ici aux cas les plus typiques. On considérera avant tout les dérivés monocycliques en ne citant que quelques exemples particulièrement importants de composés polycycliques. La nomenclature est aujourd'hui à peu près systématisée, bien qu'un grand nombre de composés hétérocycliques courants portent des noms particuliers, adoptés par l'usage.
La nature des hétéroatomes présents dans le cycle est indiquée par un préfixe : oxa- (oxygène) ; thia- (soufre) ; séléna- (sélénium) ; aza- (azote) ; phospha- (phosphore) ; sila- (silicium) ; bora- (bore).
Le nombre des chaînons du cycle est indiqué par la racine : -ir- = 3 ; -et- = 4 ; -ol- = 5 ; -in- = 6 ; -ep- = 7 ; -oc- = 8 ; -on- = 9 ; -ec- = 10.
Le degré d'insaturation est indiqué par un suffixe qui varie avec la taille du cycle et la nature des hétéroatomes. Le tableau résume les principaux noms usuels d'hétérocycles, et la figure donne quelques exemples de nomenclature. On trouvera les règles de nomenclature et de numérotage des hétérocycles dans les ouvrages cités dans la bibliographie.
On suivra l'usage le plus répandu en se référant successivement pour les monocycles aux trois paramètres : nombre de chaînons, nombre d'hétéroatomes, degré d'insaturation puis homologues polycycliques. Les hétérocycles monocycliques les plus nombreux comportent cinq ou six chaînons et un, deux et plus rarement trois ou quatre hétéroatomes. Ceux d'entre eux qui sont entièrement ou partiellement saturés ont des propriétés physiques et chimiques généralement assez voisines de celles de leurs analogues à chaîne ouverte.[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jacques METZGER : professeur de chimie organique à la faculté des sciences de Marseille
Classification
Pour citer cet article
Jacques METZGER. HÉTÉROCYCLES [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Article mis en ligne le et modifié le 14/03/2009
Médias
Autres références
-
ALCALOÏDES
- Écrit par Jacques E. POISSON
- 5 686 mots
- 5 médias
...catégorie définie de composés chimiques en raison de la variété de leurs structures moléculaires. Toutefois, d'une façon constante, ils possèdent un squelette hétérocyclique azoté, si l'on excepte quelques substances où l'azote est extracyclique (colchicine, éphédrine). La classification la plus accessible est... -
AROMATICITÉ
- Écrit par André JULG
- 4 706 mots
- 2 médias
De même, une molécule aromatique peut contenir des hétéroatomes. Par exemple, dans la pyridine C5H5N (formule 6), qui dérive formellement du benzène par le remplacement d'un groupement CH par un atome d'azote, c'est ce dernier qui fournit un électron au système conjugué. -
AZÉTIDINE ou TRIMÉTHYLÈNE-IMINE
- Écrit par Dina SURDIN
- 64 mots
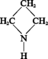
Masse moléculaire : 57,09 g
Masse spécifique : 0,843 g/cm3
Point d'ébullition : 63 0C.
Liquide incolore, fumant à l'air, d'odeur ammoniacale, soluble en toutes proportions dans l'eau et l'éthanol.
Le cycle à quatre chaînons s'ouvre facilement ; sous l'action de l'acide...
-
AZIRIDINE ou AZACYCLOPROPANE ou DIMÉTHYLÈNIMINE
- Écrit par Dina SURDIN
- 159 mots

Masse moléculaire : 43,07 g
Masse spécifique : 0,832 g/cm3
Point d'ébullition : 56 0C
Huile à très forte odeur ammoniacale, fumant à l'air. Miscible à l'eau, soluble dans l'éthanol.
Également appelée azacyclopropane, diméthylènimine ou bien cyclodiméthylène amine, l'aziridine...
- Afficher les 20 références






