DÉTERGENTS
Aspects physico-chimiques
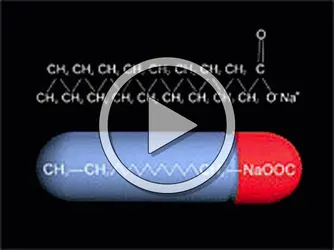
Les tensioactifs sont des molécules amphiphiles, constituées d'une queue hydrophobe et d'une tête polaire hydrophile. Cette structure chimique leur confère une grande activité aux interfaces où ils ont tendance à s'adsorber. À la surface, les molécules sont soumises à un champ de forces asymétrique dont la résultante tend à les déplacer vers l'intérieur. À l'échelle macroscopique, cette force agit de façon à minimiser la surface libre en contact avec l'air. Le champ de forces en surface peut être représenté par une quantité d'énergie libre superficielle, appelée tension superficielle. Dans le cas de deux liquides non miscibles ou d'un solide et d'un liquide, la frontière qui les sépare est appelée interface. L'énergie libre par unité de surface est la tension interfaciale.
Dans l'eau, les molécules de tensioactifs s'associent et forment des agrégats ordonnés appelés micelles car, dans l'état aggloméré, les parties hydrophobes sont dans une situation énergétique plus favorable et le système est plus stable. La formation des micelles ou micellisation apparaît à partir d'une concentration donnée appelée concentration micellaire critique (C.M.C.).
On distingue les tensioactifs anioniques (carboxylates ou savons, sulfonates d'alkylbenzènes, sulfates d'alcool gras), cationiques (dérivés d'ammoniums quaternaires), non ioniques (alcools gras polyéthoxylés) et amphotères, dont la charge dépend du pH.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Louis HO TAN TAÏ : ingénieur consultant
- Véronique NARDELLO-RATAJ : docteur de l'université de Lille-I, professeur des Universités
Classification
Pour citer cet article
Louis HO TAN TAÏ et Véronique NARDELLO-RATAJ. DÉTERGENTS [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Média
Autres références
-
ANTIBIOTIQUES
- Écrit par Aurélie CHABAUD, Sylvain MEYER, Marie-Cécile PLOY
- 6 760 mots
- 6 médias
Quant aux détergents, ce sont des produits nettoyants qui décollent les souillures de leur substrat. Ils sont destinés aux surfaces et matériaux inertes. Ils ne contiennent pas d’agent antibactérien mais contribuent à l’élimination de bactéries et du biofilm bactérien par le décollement et la dissolution... -
COLLOÏDES
- Écrit par Didier ROUX
- 6 009 mots
L'application industrielle la plus importante des solutions colloïdales stables concerne le domaine des détergents. Dissoudre des corps hydrophobes (graisses, poussières, pigments, etc.) est la caractéristique des solutions micellaires. Les propriétés de surface de ces solutions sont aussi importantes.... -
EXTRÉMOPHILES
- Écrit par Jacques DIETRICH, Jean GUEZENNEC
- 2 856 mots
C'est dans les années 1960 qu'est apparue la première protéase d'origine bactérienne dans les lessives. La recherche s'est ensuite orientée vers d'autres types de protéases, mais également de lipases (pour les taches dues aux huiles et aux graisses), d'amylases (nettoyage des taches produites par... -
INTERFACES
- Écrit par Simone BOUQUET, Jean-Paul LANGERON
- 8 287 mots
- 8 médias
Un corps tensioactif peut également conférer à un liquide un pouvoir mouillant vis-à-vis du solide s'il peut s'y lier. C'est ainsi qu'un détergent, dont la queue hydrophobe peut adhérer au tissu, va également se fixer sur les particules de graisse déposées sur celui-ci. Les têtes hydrophiles tendent...
Voir aussi
- TEXTILES FIBRES
- ENZYMES
- LESSIVES
- CMC (concentration micellaire critique)
- CHIMIQUES INDUSTRIES
- BLANCHIMENT
- LAVAGE
- EAU OXYGÉNÉE (peroxyde d'hydrogène)
- SAVONS
- ALKYLBENZÈNE SULFONATES
- TENSIOACTIVES SUBSTANCES
- TENSION SUPERFICIELLE
- AMPHIPHILE MOLÉCULE
- DÉGRAISSANTS
- PHOSPHATES
- SAPONIFICATION
- AZURAGE
- CHIMIE HISTOIRE DE LA
- PROTÉASES
- GRAISSES