SOLVANTS
Les techniques de séparation
Les techniques de séparation constituent un domaine où l'utilisation des solvants continue d'apporter des progrès importants, sur le plan analytique comme sur le plan préparatif.
Dans l' extraction liquide-liquide, on met en contact deux solutions non miscibles, l'une étant en général une solution aqueuse et l'autre une solution dans un solvant peu dissociant. Chaque soluté à extraire se partage entre les deux phases, l'équilibre étant caractérisé par un coefficient de distribution égal au rapport des concentrations dans chacune des phases.
On peut favoriser sélectivement le passage d'un soluté d'une phase dans l'autre, par exemple de la phase aqueuse à la phase organique, en ajustant la composition de l'une ou l'autre des solutions par la mise en œuvre de réactions acide-base, par la formation de complexes ou de paire d'ions. Le soluté peut ensuite être de nouveau extrait par une solution aqueuse de composition différente. La prise en compte des propriétés des solutés permet des séparations extrêmement sélectives. Les premières applications industrielles en métallurgie extractive sont nées de l'industrie nucléaire : la purification de l'uranium à partir des solutions nitriques des minerais a été obtenue par extraction par le tributylphosphate dilué avec du décane. La méthode est maintenant d'un emploi très général ; ainsi, les terres rares sont extraites sélectivement de solutions aqueuses par des acides alkyl-phosphoriques.
L'industrie pharmaceutique fait également appel aux techniques d'extraction par solvant (par exemple, extraction d'antibiotiques obtenus par fermentation), l'industrie alimentaire également. L'utilisation de solvants dits hypercritiques, comme le dioxyde de carbone liquide sous pression, offre des solutions élégantes et peu polluantes pour l'extraction de substances thermosensibles comme la caféine, les acides gras, les hormones naturelles.
De nouvelles méthodes de synthèse en chimie organique mettent en œuvre la catalyse par transfert de phase dans laquelle un réactif est transféré de l'une des phases (généralement la phase aqueuse) dans la phase organique où il réagit grâce à la formation d'une paire d'ions avec un cation (ammonium quaternaire, cryptate alcalin) en faible concentration.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jacques DEVYNCK : directeur de recherche au C.N.R.S.
Classification
Pour citer cet article
Jacques DEVYNCK. SOLVANTS [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Article mis en ligne le et modifié le 14/03/2009
Média
Autres références
-
ACÉTONE
- Écrit par Roger GALLO
- 641 mots
Liquide volatil incolore, d'une odeur piquante, miscible avec l'eau, l'alcool, l'éther, le chloroforme et le benzène, l'acétone, ou diméthylcétone, ou propan-2-one, a pour formule brute C3H6O : un atome de carbone C est lié par des liaisons chimiques simples à deux...
-
ACÉTYLÈNE
- Écrit par Henri GUÉRIN
- 5 089 mots
- 6 médias
...l'extension, lorsque les travaux de Linde et de Claude eurent fourni la possibilité d'extraire facilement l'oxygène de l'air. La préparation de solvants chlorés : trichloréthylène et perchloréthylène, entreprise dès 1910 en Allemagne, ne devait surtout se développer en France et dans les autres... -
ACIDES & BASES
- Écrit par Yves GAUTIER et Pierre SOUCHAY
- 12 364 mots
- 7 médias
En raison de sa charge élevée par rapport à son volume, H+ n'existe pas comme tel en solution, mais se fixe sur le solvant (dénommé SH) qui se trouve jouer ainsi le rôle de base. Par conséquent, l'ionisation d'un acide dans l' eau ne s'écrira pas :mais :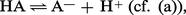 et la constante...
et la constante...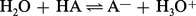
-
ALCOOL ÉTHYLIQUE ou ÉTHANOL
- Écrit par Fernand COUSSEMANT
- 694 mots
Alcool primaire, liquide incolore, d'odeur agréable, miscible à l'eau en toutes proportions, miscible à de nombreux solvants organiques, l'éthanol ou alcool éthylique, CH3—CH2OH, a les caractéristiques suivantes :
Masse moléculaire : 46,07 g
Masse spécifique : 0,789 3...
- Afficher les 45 références



