ASTROCHIMIE
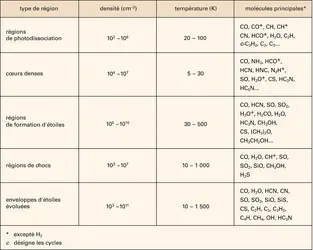
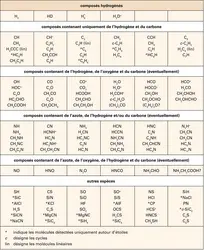
Dans les années 1960, l'espace intersidéral était encore considéré comme un environnement vide, hostile et stérile. Suivant en cela Arthur Stanley Eddington (1926), les astrophysiciens de l'époque jugeaient « difficile d'admettre l'existence de molécules dans l'espace interstellaire, parce qu'une fois qu'une molécule est dissociée il semble n'y avoir aucune chance pour que les atomes se joignent à nouveau ». Le gaz était décidément trop ténu entre les étoiles, et trop baigné de rayonnements destructeurs, pour que des molécules s'y forment. Même la présence dans l'espace de CH, CN et CH+ – trois « exceptions » détectées en 1937, 1940 et 1941, respectivement – s'expliquait par la désagrégation, dans le gaz, de molécules formées sur des grains de poussière interstellaire, ces solides microscopiques qui obscurcissent le rayonnement des étoiles. L'Univers, finalement, demeurait désert. Mais les choses ont bien changé. Depuis la fin des années 1960, plus de 140 espèces moléculaires ont été repérées dans l'espace. Acétylène, ammoniac, méthanol, vapeur d'eau, par exemple, sont ainsi couramment détectés dans le milieu interstellaire. Mieux, on a découvert entre les étoiles des molécules jusqu'ici inconnues sur Terre. C'est que, loin d'être vide et stérile, l'espace intersidéral est en fait le siège d'une florissante chimie, atypique et diversifiée.
Les méthodes de l'astrochimie
Comme les autres chercheurs en astronomie, l'astrochimiste obtient des informations sur l'Univers en analysant son rayonnement, depuis la Terre ou depuis l'espace. La spectroscopie se révèle ainsi indispensable pour identifier les différentes molécules, déterminer leurs abondances ou encore mesurer les propriétés du milieu où elles se forment. C'est la méthode reine de l'astrochimie. Pour reconnaître les atomes, les ions et les molécules présentes dans le milieu interstellaire, l'ensemble du spectre électromagnétique est exploité. Néanmoins, les radiotélescopes, comme ceux de l'Institut de radioastronomie millimétrique (Iram), sont particulièrement adaptés, car la plupart des émissions moléculaires de basse énergie (qui correspondent au mouvement de rotation des molécules sur elles-mêmes) se placent dans le domaine des longueurs d'onde millimétriques. Le domaine infrarouge, de plus haute énergie (mouvement de vibration des molécules), a été exploité par le satellite I.S.O. (Infrared Space Observatory) de l’Agence spatiale européenne (E.S.A.), opérationnel de novembre 1995 à mai 1998 ; le satellite de l'E.S.A. Herschel (auparavant FIRST : Far Infrared and Sub-millimetre Telescope) et l'interféromètre géant A.L.M.A. (Atacama Large Millimeter/Submillimeter Array) doivent explorer les domaines milimétrique et submillimétrique, à la frontière entre les domaines radio et infrarouge.
L'identification des espèces interstellaires par leur rayonnement serait impossible sans les calculs théoriques et les expériences de laboratoire des spectroscopistes. Ces physiciens sont souvent associés aux découvertes de nouvelles molécules dans l'espace, parfois reconnues d'abord dans leurs expériences. De nombreuses chaînes carbonées (jusqu'à HC17N, C14H, H3C15H...) ont ainsi été synthétisées dans les laboratoires, mais pas encore détectées dans l'espace. Notons que cette contribution des physiciens à l'astrochimie est payée de retour : les milieux astrophysiques offrent des conditions extrêmes, souvent difficiles à reproduire sur Terre, qui permettent d'étudier la matière dans des états exceptionnels.
La collaboration étroite entre physiciens et astronomes ne se limite pas à la spectroscopie. Calculs et travaux en laboratoire permettent aussi de déterminer les constantes[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- David FOSSÉ : journaliste scientifique
- Maryvonne GERIN : chercheur au Laboratoire d'étude du rayonnement et de la matière en astrophysique (L.E.R.M.A.), C.N.R.S., Observatoire de Paris, École normale supérieure et université de Paris-VI-Pierre-et-Marie-Curie
Classification
Pour citer cet article
David FOSSÉ et Maryvonne GERIN. ASTROCHIMIE [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
ALMA (Atacama Large Millimeter/submillimeter Array)
- Écrit par Pierre LÉNA
- 2 129 mots
- 5 médias
La chimie interstellaire est pratiquement née avec la radioastronomie millimétrique dans les années 1980. Avec A.L.M.A., elle entre dans une nouvelle phase, puisque des molécules peuvent être détectées dans tous les types d'objets, en particulier à très grande distance. La complexité des échanges physico-chimiques,... -
COMÈTES
- Écrit par Myriam DÉTRUY
- 4 347 mots
- 7 médias
Les comètes s'étant formées dans des environnements froids, à des températures inférieures à –170 0C, elles ont subi peu de modifications chimiques, sauf à leur surface si elles ont été bombardées par des rayons ultraviolets ou des protons cosmiques. Les plus gros objets ont peut-être... -
ÉTOILES
- Écrit par André BOISCHOT, Jean-Pierre CHIÈZE
- 13 456 mots
- 8 médias
La formation des molécules dans un nuage peut conduire à sa fragmentation. Les molécules ne peuvent se former que lorsque la densité, à la suite de la contraction globale du nuage, a atteint une valeur suffisamment élevée (plusieurs atomes par mètre cube). La formation de molécules comme H... -
INTERSTELLAIRE MILIEU
- Écrit par James LEQUEUX
- 3 696 mots
- 4 médias
...peu ou pas d'hydrogène atomique (détectable par la raie à 21 cm), mais il n'est malheureusement observable que dans des circonstances exceptionnelles. Contrairement à la plupart des autres molécules, celles d'hydrogène ne peuvent se former à partir des atomes d'hydrogène que par catalyse sur les grains.... - Afficher les 7 références
Voir aussi