DYNAMIQUE MOLÉCULAIRE
- 1. Une nouvelle composante de la connaissance des structures des molécules
- 2. Notions de structure en solution
- 3. Une méthode privilégiée pour l'étude de la dynamique moléculaire : la résonance magnétique nucléaire
- 4. Libre rotation autour d'une liaison
- 5. La pyramide trigonale
- 6. L'inversion du tétraèdre
- 7. La pseudorotation des coordinats autour d'un élément pentacoordiné
- 8. Complexes octaédriques
- 9. Nombres de coordination plus élevés
- 10. Les composés organométalliques : des structures très turbulentes
- 11. Macromolécules et biopolymères
- 12. Bibliographie
L'inversion du tétraèdre
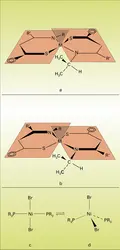
Le carbone tétraédrique, c'est-à-dire l'atome de carbone porteur de quatre substituants disposés aux sommets d'un tétraèdre, est l'unité constituante de base des molécules organiques. Il est caractérisé par une grande rigidité stéréochimique : on a estimé que l'inversion d'une molécule de méthane, CH4, se produit en moyenne tous les 10 000 ans ! Dans la pratique, un carbone tétraédrique ne s'inverse pas sans rupture de liaison. Cette rigidité ne se retrouve pas dans les dérivés tétracoordinés de la plupart des autres éléments, pour lesquels l'inversion du tétraèdre est souvent très rapide, trop rapide pour permettre la séparation des deux molécules isomères, images l'une de l'autre dans un miroir, que l'on obtient lorsque les quatre substituants sont tous différents. C'est le cas par exemple des deux molécules montrées en (où M est un atome de zinc ou de cadmium), qui peuvent être assimilées à deux hélices, l'une tournant à droite, l'autre à gauche, mais dont les pas s'inverseraient un grand nombre de fois par seconde à la température ambiante. Au cours de cette inversion, il arrive un moment où l'atome M et ses quatre substituants sont coplanaires ; dans le cas du zinc et du cadmium, cette disposition est défavorisée, tant pour des raisons de plus grand encombrement stérique que pour des raisons électroniques, et correspond au sommet de la barrière d'énergie qu'il faut franchir pour que l'inversion se produise.
Dans d'autres cas, lorsque l'état plan est stabilisé par certains facteurs électroniques (effets du champ des coordinats) et devient d'énergie comparable à celle du composé tétraédrique, l'atome tétracoordiné peut adopter les deux géométries, tétraédrique et plane ; toutes deux correspondent à des puits de potentiel. Il arrive alors que l'on puisse obtenir et isoler les deux formes, c'est-à-dire deux molécules de même composition, et présentant les mêmes connections interatomiques, mais différant par les angles interatomiques et donc dans leurs propriétés. Les composés c, plan et diamagnétique, et d, tétraédrique et paramagnétique, en sont un exemple : ils ont pu être séparés, conservent leur structure indéfiniment dans l'état solide, mais s'interconvertissent à un rythme rapide dès qu'ils sont mis en solution.
- 1. Une nouvelle composante de la connaissance des structures des molécules
- 2. Notions de structure en solution
- 3. Une méthode privilégiée pour l'étude de la dynamique moléculaire : la résonance magnétique nucléaire
- 4. Libre rotation autour d'une liaison
- 5. La pyramide trigonale
- 6. L'inversion du tétraèdre
- 7. La pseudorotation des coordinats autour d'un élément pentacoordiné
- 8. Complexes octaédriques
- 9. Nombres de coordination plus élevés
- 10. Les composés organométalliques : des structures très turbulentes
- 11. Macromolécules et biopolymères
- 12. Bibliographie
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jean RIESS : professeur à l'université de Nice-Sophia Antipolis, directeur de l'unité de chimie moléculaire associée au C.N.R.S.
Classification
Pour citer cet article
Jean RIESS. DYNAMIQUE MOLÉCULAIRE [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
BIOPHYSIQUE
- Écrit par Claude Michel GARY-BOBO
- 6 413 mots
...modernes permettent de traiter d'importants ensembles d'informations de ce type. La difficulté provient du fait, rapidement reconnu par cette approche, qu'une molécule, même lorsqu'elle n'est pas très grande, ne se trouve pas sous une forme ou configuration unique, mais qu'elle oscille sans cesse entre... -
CRISTAUX LIQUIDES
- Écrit par Henry GASPAROUX
- 4 816 mots
- 9 médias
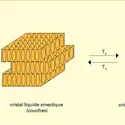
...à des bâtonnets cylindriques ou à des ellipsoïdes. Ces modèles ont conduit à une bonne description des propriétés des phases smectiques et nématiques. On essaie actuellement, à l'aide des techniques spectroscopiques habituelles, de dépasser et d'affiner ce type de description afin de savoir quelle est... -
MOLÉCULE
- Écrit par André JULG
- 4 301 mots
Si l'hypersurface présente plusieurs minimums énergétiquement bien séparés, à chacun d'eux correspond une molécule. Les diverses molécules ainsi définies possèdent la même formule brute et sont dites isomères. La série des sucres nous offre de très nombreux cas d'isomérie. Par... -
TAUTOMÉRIE
- Écrit par Bernard CARTON
- 137 mots
Cas particulier de transposition intramoléculaire, résultant de réarrangements rapides et réversibles (isomérie dynamique). Plus précisément, on appelle ainsi la transformation d'un corps chimique en un isomère différent du premier par l'emplacement d'un atome et par la disposition des liaisons, cette...
Voir aussi
- FRÉQUENCE, physique
- SPECTROCHIMIQUE ANALYSE
- ÉTHYLÈNE
- PIC, chimie analytique
- SITE DE FIXATION
- ÉNERGIE D'ACTIVATION
- RMN (résonance magnétique nucléaire), physico-chimie
- SUBSTITUTION, chimie
- ORBITALES MOLÉCULAIRES
- LIBRE ROTATION, chimie
- CRISTALLOCHIMIE
- TÉTRAÈDRE, stéréochimie
- OCTAÈDRE, stéréochimie
- SOLUTION, chimie
- PROTÉINES
- COORDINATION COMPOSÉS DE