MERCURE, élément chimique
Le mercure, élément chimique de numéro atomique 80, est le seul métal liquide à la température ordinaire. Il tire son symbole Hg du mot grec latinisé hydrargyrum (argent liquide). Le mot actuel a été introduit au vie siècle par les alchimistes qui le représentaient par le symbole de la planète Mercure. L'ancien nom français vif-argent est conservé en allemand (Quecksilber). Le mercure appartient avec le zinc et le cadmium aux éléments du groupe IIb du tableau périodique. À l'état fondamental, sa structure électronique est caractérisée par une sous-couche 5d saturée et par la présence d'un doublet électronique en 6s. Tandis que les éléments de la colonne Ib (Cu, Ag, Au) peuvent perdre un ou deux électrons d pour donner des ions ou des complexes aux degrés d'oxydation + II et + III, cela n'est plus possible pour les éléments IIb et tout particulièrement pour le mercure dont le degré d'oxydation maximal sera de II. Les orbitales 5d des couches saturées de l'atome de mercure n'interviennent jamais dans la formation des liaisons. L'inertie totale de la sous-couche 5d est une propriété caractéristique du mercure. Pour cette raison, il ne sera pas considéré comme élément de transition bien qu'il possède quelques analogies avec ceux-ci, en particulier la formation de nombreux complexes de coordination. Les propriétés du mercure sont liées à la tendance des seuls électrons 6s à donner des liaisons. Ces électrons étant relativement inertes, la réactivité chimique de l'élément est faible.
Préparation
La production mondiale annuelle de mercure est passée d'un maximum de 10 000 tonnes en 1970 à 6 500 tonnes en 1986, 3 260 tonnes en 1996 et 1 600 tonnes en 2003, en provenance principalement d'Espagne, du Kirghizstan, de Chine, et d'Algérie.
Le mercure se rencontre à l'état naturel essentiellement sous forme de sulfure rouge appelé « cinabre ». Très simple, l'extraction à partir du cinabre s'effectue par grillage du minerai à l'air :
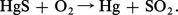
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Guy PÉREZ : professeur à la faculté des sciences de Rouen (chimie des solides)
- Jean-Louis VIGNES : professeur d'université à l'I.U.F.M. de Créteil, chercheur au Centre d'études de chimie métallurgique (C.N.R.S.)
Classification
Pour citer cet article
Guy PÉREZ et Jean-Louis VIGNES. MERCURE, élément chimique [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
MERCURE, toxicologie
- Écrit par Universalis
- 578 mots
Certaines industries modernes mais aussi des processus biologiques aboutissent à une concentration dangereuse des composés mercuriels dans l'organisme humain. Le mercure est largement utilisé dans l'industrie, les produits chimiques, les peintures, divers objets, des pesticides et des...
-
ALCHIMIE
- Écrit par René ALLEAU, Universalis
- 13 642 mots
- 2 médias
...effet, compliquées et dispendieuses, en dépit de leur simplicité apparente : la préparation et l'absorption du cinabre (dan), un sulfure naturel rouge de mercure. À vrai dire, l'expression même de cinabre mâle (yangdan) qui désignait le procédé alchimique par différence avec le nom de cinabre... -
AMÉRIQUE (Histoire) - Amérique espagnole
- Écrit par Jean-Pierre BERTHE
- 21 855 mots
- 13 médias
... siècle, à San Luis Potosí, sur le plateau central mexicain. Mais l'extraction de l' argent est relancée par le procédé de l'amalgame au mercure, mis au point en Nouvelle-Espagne en 1555-1556, au moment même où tarissent un peu partout les premiers filons à grand rendement. Dès 1562-1563,... -
CHLORE
- Écrit par Henri GUÉRIN
- 5 625 mots
- 5 médias
On utilise une cathode circulante en mercure au contact de laquelle le sodium formé s'amalgame tandis que le chlore se dégage ; le mercure contenant environ 0,2 p. 100 de sodium s'écoule de la cellule et passe dans un décomposeur dans lequel il fournit, en présence d'eau, de l'hydrogène et de la soude.... -
CYCLES BIOGÉOCHIMIQUES
- Écrit par Jean-Claude DUPLESSY
- 7 878 mots
- 6 médias
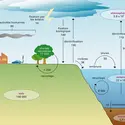
Le cycle naturel du mercure (Hg) est dominé par le transport atmosphérique et les échanges entre l'atmosphère et la surface des continents ou des océans. Ce métal est relâché par les volcans et par volatilisation depuis les terres et les mers. Ses temps de résidence dans l'atmosphère, les sols et l'océan... - Afficher les 18 références
Voir aussi