PLUTONIUM
Élément chimique artificiel de numéro atomique 94, le plutonium a pour symbole chimique Pu. Par analogie avec les éléments uranium et neptunium le précédant immédiatement dans la classification périodique, il doit son nom à la planète Pluton découverte après Uranus et Neptune.
Le plutonium fut découvert en 1940 à l'université de Californie par une équipe dirigée par Glenn T. Seaborg. La réaction nucléaire de synthèse mettait en jeu le bombardement d'une cible d'oxyde d'uranium par des deutons de 16 MeV accélérés dans un cyclotron. La réaction nucléaire conduit à l'isotope de masse 238 du neptunium, émetteur β— dont la demi-vie radioactive est de 2,117 j. Le plutonium 238 obtenu par les réactions ci-dessous est caractérisé par une radioactivité α d'une demi-vie de 87,7 ans :
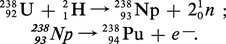
De nombreux isotopes furent ensuite synthétisés, en particulier l'isotope 239. En 1941, la démonstration du caractère fissile de celui-ci lors de l'irradiation par des neutrons lents inaugurait le début d'une production à grande échelle, d'une part à des fins militaires (qui devait aboutir en 1945 à l'explosion nucléaire de Nagasaki), d'autre part à des fins civiles, comme combustible dans les réacteurs nucléaires.
Le tableau résume les caractéristiques nucléaires des principaux isotopes (20 sont répertoriés actuellement). En plus des modes de désintégration indiqués, ces isotopes se fissionnent spontanément avec des périodes voisines de 1010 ans pour ceux dont la masse est paire et de plus de 1015 ans pour le 239Pu.
Production
Deux isotopes, le plutonium 239 et le plutonium 238, ont reçu des applications justifiant une production importante pour le premier, beaucoup plus limitée pour le second. Ces productions, effectuées dans le cadre de programmes nationaux souvent couverts par le secret militaire, ne peuvent être évaluées avec précision.
Plutonium 239
Le plutonium 239 se forme dans les réacteurs nucléaires alimentés à l' uranium. La capture radiative d'un neutron par l'uranium 238 conduit à un isotope de masse supérieure, l'uranium 239. Celui-ci, instable, se transmute par émission β— en neptunium 239 avec une demi-vie de 23,45 minutes. Ce dernier isotope est également émetteur β— (sa demi-vie est de 2,356 j) ; il donne naissance au plutonium 239, émetteur α d'une demi-vie de 24 110 ans.
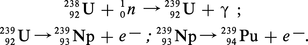
Au cours du fonctionnement du réacteur, il s'opère donc une transmutation de 238U en 239Pu qui s'accumule dans le combustible. Du fait de ses caractéristiques nucléaires, une partie du plutonium 239 subit la fission par les neutrons et une autre partie donne naissance par capture neutronique aux isotopes supérieurs 240, 241 et 242 selon les réactions nucléaires suivantes :
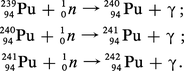
La proportion relative des isotopes du plutonium dans le combustible varie avec l'enrichissement de l'uranium, les conditions d'irradiation (en particulier, l'énergie des neutrons) et le taux d'irradiation.
Ainsi, dans le combustible d'un réacteur à eau pressurisée caractérisé par un enrichissement initial de l'uranium de 3,5 p. 100 et un taux d'irradiation de 33 000 MW.j.t—1, la masse de plutonium est voisine de 1 p. 100 de celle de l'uranium. La composition isotopique de ce plutonium indique la présence de 50 à 60 p. 100 d'isotope 239 et de quantités décroissantes des isotopes suivants jusqu'au plutonium 242. On peut noter également une contribution de 1 à 2 p. 100 de l'isotope 238 formé par réaction nucléaire sur le 237Np produit pendant l'irradiation.
Dans ce même type de combustible, la masse des produits de fission est voisine de 3,5 p. 100 de la masse d'uranium. Ceux-ci émettent un flux de rayonnements β— et γ très important. En raison de cette activité considérable, les opérations[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Daniel CALAIS : chef honoraire de la section de métallurgie du plutonium et des actinides au Commissariat à l'énergie atomique
- André CHESNÉ : ingénieur de l'École supérieure de physique et chimie industrielle de la Ville de Paris, assistant de directeur au Commissariat à l'énergie atomique, directeur de laboratoire au Centre de recherche de l'École centrale des arts et manufactures
Classification
Pour citer cet article
Daniel CALAIS et André CHESNÉ. PLUTONIUM [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Article mis en ligne le et modifié le 25/03/2009
Médias
Autres références
-
AMÉRICIUM
- Écrit par Monique PAGÈS
- 1 385 mots
...dans les combustibles nucléaires, où il peut être récupéré au cours de leur traitement chimique. Il se trouve mélangé à de nombreux autres éléments : le plutonium 239 ou l'uranium (c'est-à-dire le combustible) existent en quantités généralement importantes ; on trouve aussi les produits de fission et d'autres... -
ARMES - Armes lourdes
- Écrit par Alain BRU
- 3 925 mots
- 2 médias
À masse égale réagissante, la fission de l'uranium 235 ou duplutonium 239 est dix-huit millions de fois plus énergétique que celle d'un explosif courant, comme le T.N.T. (trinitrotoluène). Mais la rapidité de l' explosion met si vite la charge fissile en configuration non critique que le... -
CURIUM
- Écrit par Marc LEFORT et Monique PAGÈS
- 1 228 mots
...travaillant au Metallurgical Laboratory de l'université de Chicago, isolèrent pendant l'été 1944 le premier isotope de l'élément 96 à partir de cibles de plutonium 239 bombardées par des noyaux d'hélium (particules alpha) accélérés au cyclotron de Berkeley (université de Californie). Le nouveau nucléide... -
MANHATTAN PROJECT
- Écrit par Georges KAYAS
- 671 mots
- 6 médias
- Afficher les 17 références




