OZONE ATMOSPHÉRIQUE
En 1995, le prix Nobel de chimie a été attribué à Paul Crutzen, Mario Molina et F. Sherwood Rowland pour leurs travaux sur les processus qui modifient l'abondance de l'ozone dans les différentes couches de l'atmosphère. Dès les années 1970, les scientifiques avaient soulevé le risque de la destruction de l'ozone stratosphérique par des produits issus de l'activité humaine. Cette alerte a fini par conduire les décideurs politiques et les industriels à abandonner une technologie florissante. Ainsi, par crainte des conséquences à l'échelle globale, on aura mis fin à une « expérience » involontaire constituée par l'introduction de chlorofluorocarbures (CFC) dans l'atmosphère.
La nature aura par ailleurs perturbé la stratosphère lors de l'éruption spectaculaire du Pinatubo (Philippines) en 1991, à un moment où la curiosité et les appréhensions des chercheurs, l'activité des médias et les craintes du public avaient conduit à la mise en place d'importants moyens d'étude de l'atmosphère. Cependant, le problème de l'ozone est au moins double, sinon triple, car si ce gaz joue un rôle d'écran protecteur dans la stratosphère en absorbant les rayons ultraviolets (U.V.), il constitue un polluant toxique dans la troposphère, et il participe aussi à l'effet de serre.
Découverte de l'ozone atmosphérique
L'ozone (O3), découvert en laboratoire en 1839 par le chimiste souabe Christian Friedrich Schönbein (1799-1868), est un gaz à l'odeur âcre que l'on peut détecter lors de sa formation dans les décharges électriques (foudre, courts-circuits, etc.). Ce gaz est le seul constituant atmosphérique capable de filtrer le rayonnement U.V. entre 240 et 300 nanomètres (1 nanomètre = 10–9 m) de longueur d'onde. Cet intervalle fixe la limite effective dans l'ultraviolet du spectre solaire observé du sol. De ce fait, l'ozone nous protège des photons énergétiques capables de désorganiser les molécules complexes du vivant. De plus, l'ozone contribue à l'effet de serre par sa bande d'absorption à 9,6 micromètres (1 micromètre = 10–6 m) de longueur d'onde, au milieu de la « fenêtre » infrarouge atmosphérique.
La mesure de la concentration de l'ozone dans l'air ambiant commence dès 1840, d'abord pour des raisons médicales. La surveillance de la quantité totale d'ozone présente dans l'atmosphère se fait depuis le début du xxe siècle par la mesure à partir du sol de ses bandes d'absorption U.V. dans le spectre solaire (ou lunaire). Cette quantité totale est très faible : si l'on pouvait ramener tout l'ozone présent dans l'atmosphère aux conditions de pression au niveau de la mer, cela ne ferait qu'une couche d'ozone pur d'une épaisseur d'environ 3 millimètres en moyenne, soit 300 unités Dobson (D.U.) pour honorer l'inventeur du spectrophotomètre utilisé pour ces mesures.
La concentration de l'ozone dans l'air se mesure directement au sol, ou en altitude avec des instruments installés à bord d'avions ou de ballons. Elle varie d'une à quelques dizaines de parties par milliard (ppb) par unité de volume dans la troposphère, et s'établit à un niveau de cent à cinq cents fois plus important, mais néanmoins encore très faible (quelques parties par million ou ppm), dans la stratosphère. L'ozone, qui se trouve donc à 90 p. 100 dans la stratosphère, joue un rôle fondamental dans le maintien de la structure de celle-ci, car son absorption du rayonnement proche U.V. solaire constitue une source de chaleur en altitude. À partir de la tropopause, limite (située entre 8 et 15 km d'altitude, selon la latitude et la saison) entre la troposphère et la stratosphère, la température augmente ainsi avec l'altitude. En revanche, dans la troposphère, où la principale source de[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Robert KANDEL : directeur de recherche honoraire du C.N.R.S., laboratoire de météorologie dynamique, École polytechnique, Palaiseau
Classification
Pour citer cet article
Robert KANDEL. OZONE ATMOSPHÉRIQUE [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Article mis en ligne le et modifié le 10/02/2009
Médias
Autres références
-
TROU DANS LA COUCHE D'OZONE
- Écrit par Florence DANIEL
- 315 mots
- 1 média
L'ozone (O3) situé dans la stratosphère joue un rôle protecteur en absorbant les rayons ultraviolets. Une diminution de sa teneur a pour conséquence d'augmenter le bombardement de la surface terrestre par les U.V., ce qui a des effets néfastes sur tous les êtres vivants.
En 1974,...
-
AÉRONOMIE
- Écrit par Gaston KOCKARTS
- 4 157 mots
- 11 médias
...pour assurer la conservation de l'énergie :Dans la stratosphère, il existe une autre réaction très efficace :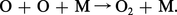 donnant lieu à la formation de l' ozone (O3). Cependant, les molécules d'ozone peuvent être détruites par la réaction :
donnant lieu à la formation de l' ozone (O3). Cependant, les molécules d'ozone peuvent être détruites par la réaction :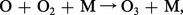 ou peuvent être photodissociées suivant le processus :...
ou peuvent être photodissociées suivant le processus :...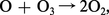
-
AIR
- Écrit par Jean PERROTEY
- 2 154 mots
- 2 médias
...moins en partie, régulée par sa dissolution dans l'eau et par la présence d'énormes masses de calcaires à la surface du globe. Le protoxyde d'azote et l'ozone sont synthétisés dans la haute atmosphère, à une altitude supérieure à 25 kilomètres. L'énergie du rayonnement ultraviolet solaire est en grande... -
ANTARCTIQUE
- Écrit par Pierre CARRIÈRE , Edmond JOUVE , Jean JOUZEL , Gérard JUGIE et Claude LORIUS
- 16 481 mots
- 24 médias
Formé de trois atomes d'oxygène, l'ozone (O3) est un constituant présent dans l'atmosphère en très faible quantité, équivalente à une épaisseur de quelques millimètres dont environ 90 p. 100 entre 20 et 50 kilomètres d'altitude. Son rôle est cependant essentiel, car il absorbe très efficacement... -
ATMOSPHÈRE - La couche atmosphérique terrestre
- Écrit par Jean-Pierre CHALON
- 7 816 mots
- 7 médias
...0,93 p. 100 pour l’argon) conservent une proportion quasiment constante jusqu’à une altitude proche de 80 à 100 kilomètres. Les proportions moyennes en ozone font exception à cette règle : alors qu’elles ne dépassent pas 5 × 10-6 p. 100 (soit 50 molécules d’ozone par milliard de molécules d’air)... - Afficher les 29 références






