ÉTHERS-OXYDES
Le chauffage, vers 140 0C, d'un mélange d'alcool vini (éthanol) et d'huile de vitriol (acide sulfurique) avait permis aux chimistes du xviiie siècle l'isolement d'un liquide très volatil, d'odeur forte, auquel ils donnèrent d'abord le nom d'« éther sulfurique ». Plus tard, ce composé fut désigné sous les noms d'« éther des pharmaciens », d'« éther ordinaire », d'oxyde d'éthyle et d'éthoxyéthane (officiellement). C'est, sinon le plus simple, du moins le plus important d'une série de composés résultant de l'élimination d'eau entre deux molécules d' alcools identiques ou différents : R−O−R ou R−O−R′, désignés sous le nom d'éthers-oxydes, et, plus récemment, sous le nom d'éthers ; le nom a été étendu à des composés provenant de l'élimination d'une molécule d'eau entre un phénol et un alcool, ou entre deux phénols, identiques ou différents :

Ce sont, en général, des liquides très stables thermiquement et chimiquement ; plusieurs, dont l'oxyde d'éthyle, sont ainsi employés comme solvants d'extraction et solvants réactionnels. Ils jouent un rôle fondamental dans la préparation des composés organométalliques, en particulier des organomagnésiens. L'oxyde d'éthyle a été longtemps employé comme anesthésique.
Les éthers-oxydes cycliques présentent des propriétés particulières, notamment les époxydes (cycles à trois sommets) très réactifs et les polyéthers cycliques (éthers-couronne) remarquables complexants des cations.
Nomenclature et préparations
Les éthers-oxydes ou éthers dérivent de l'eau par remplacement des deux hydrogènes par deux groupements hydrocarbonés (aliphatiques, alicycliques, aromatiques). Ils peuvent être symétriques : R−O−R ou dissymétriques (mixtes) : R−O−R′. La nomenclature officielle désigne la fonction éther par le préfixe alcoxy- ou aryloxy- suivi du nom de la chaîne principale (la plus longue ou la plus ramifiée). Une nomenclature courante désigne les dérivés symétriques par le nom (di)alkyléther et les éthers mixtes par le nom éther d'alkyle et d'alkyle′ ; les éthers cycliques ont des noms particuliers dérivant de la nomenclature des hétérocycles.
Les monoéthers simples sont relativement rares dans le règne végétal : les plus communs d'entre eux dérivent de l'anisole C6H5−O−CH3. Par contre, la fonction alcoxy (méthoxy−OCH3) est très répandue dans des molécules naturelles complexes telles que la lignine, les alcaloïdes et les glucides.
Deux éthers aliphatiques symétriques, l'éther éthylique et l'éther butylique, sont préparés par déshydratation des alcools primaires correspondants, soit par H2SO4 à 120 0C, soit en catalyse hétérogène (Al2O3, à 250 0C). Ce type de préparation est pratiquement limité aux seuls alcools primaires, par suite de la tendance des alcools secondaires et tertiaires à subir, en milieu acide et à chaud, une élimination conduisant à un alcène. Cette réaction peut également se produire avec les alcools primaires, mais à température supérieure à 140 0C.
La méthode la plus générale pour obtenir des éthers est celle que Williamson a proposée en 1850, la réaction d'un alcoolate alcalin sur un halogénure d'alkyle ou d'aryle :
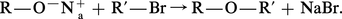
Les éthers de tertiobutyle peuvent provenir, en catalyse acide, de l'addition d'un alcool ou d'un phénol sur l'isobutène.
Les préparations des éthers cycliques sont le plus souvent dérivées de la méthode de Williamson : la[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jacques METZGER : professeur de chimie organique à la faculté des sciences de Marseille
Classification
Pour citer cet article
Jacques METZGER. ÉTHERS-OXYDES [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Article mis en ligne le et modifié le 14/03/2009
Média
Autres références
-
CARBURANTS
- Écrit par Daniel BALLERINI , Jean-Claude GUIBET et Xavier MONTAGNE
- 10 527 mots
- 9 médias
– Des composés oxygénés, du type éther (métyltertiobutyléther ou MTBE, éthyltertiobutyléther ou ETBE) ; leurs indices d'octane dépassent 110 pour le RON et 95 pour le MON ; la présence d'oxygène conférant aux essences des modifications de caractéristiques, leur teneur est limitée à 15 p. 100.... -
HALOGÈNES
- Écrit par Jacques METZGER et Robert de PAPE
- 6 600 mots
- 5 médias
L'alcoolyse conduit aux éthers, elle est voisine de l'hydrolyse : lente pour les halogénures primaires, elle est rapide pour les tertiaires. L'emploi d'un alcoolate accélère la réaction (réaction de Williamson) mais entraîne la réaction parallèle d'élimination (cf. éthers-oxydes) :
-
ORGANOMÉTALLIQUES COMPOSÉS
- Écrit par Jacques METZGER et Charles PRÉVOST
- 4 208 mots
- 2 médias
Les iodures et bromures tertiaires agissent facilement (réaction). Plus réactifs, les éthers sulfuriques, même primaires, conduisent à une condensation analogue. -
OXOLANES
- Écrit par Dina SURDIN
- 62 mots
Composés hétérocycliques à cinq chaînons, comportant un atome d'oxygène. On peut donc les considérer comme des éthers cycliques. L'exemple le plus simple en est le tétrahydrofuranne.
De la même manière, les dioxolanes comportent deux atomes d'oxygène dans un cycle à cinq chaînons...



