- 1. Généralités
- 2. Atmosphère pure et sèche
- 3. Action des constituants minoritaires
- 4. Les constituants hydrogénés et la chimie mésosphérique
- 5. Les composés oxygénés de l'azote et la chimie stratosphérique
- 6. Les composés halogénés et la chimie stratosphérique
- 7. Les sources et les puits des composés hydrogénés, azotés et halogénés
- 8. Bibliographie
ATMOSPHÈRE Chimie
Action des constituants minoritaires
Des études expérimentales montrent que l'ozone peut être réduit par l'action d'un cycle catalytique du type suivant :

X désigne un atome ou une molécule comme l'hydrogène, le monoxyde d'azote ou des radicaux hydroxyle ou perhydroxyle, ou même des atomes halogénés. Ainsi, à la réaction (5) de reformation de O2 s'ajoute l'action des réactions de l'ensemble catalytique (6). En d'autres termes, les atomes halogénés, ou tout autre constituant du même type attaquant l'ozone, sont toujours restitués par la réaction de leur oxyde avec l'atome d'oxygène et constituent ainsi un cycle permanent de destruction de l'ozone. En chimie atmosphérique, il s'agit donc de déterminer comment apparaissent de tels constituants et en même temps de fixer leur importance.
On a d'abord reconnu l'existence atmosphérique de la vapeur d'eau, H2O, du méthane, CH4, et de l'hydrogène moléculaire, H2, jusqu'à de hauts niveaux. Dans la mésosphère, on assiste à la photodissociation de H2O et de CH4 par des processus tels que :
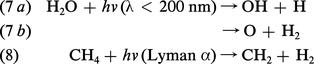
Ces processus donnent lieu à l'apparition de l'atome d'hydrogène et de l'hydroxyle. Cependant, dans la stratosphère, où la photodissociation de H2O n'apparaît pas, on doit faire appel à un autre processus dont l'ozone est responsable. Il s'agit d'un mécanisme de dissociation due à la réaction avec l'atome d'oxygène excité O(1D). On observe la production de H et de OH :

L'origine de cet atome d'oxygène excité est due à l'ozone. Sa concentration maximum dans la stratosphère ne s'élève qu'à quelque cent ou deux cents atomes par centimètre cube en présence de 1018 molécules N2 et O2. Sous l'influence de l'absorption dans la bande de Hartley pour des longueurs d'onde inférieures à 310 nm, on a en effet la production d'une molécule et d'un atome d'oxygène dans des états excités :

L'état excité O(1D) permet avec son énergie supplémentaire les réactions rapides (9), (10) et (11) qui n'auraient pas lieu avec l'atome O(3P) dans son état normal, tout au moins aux températures de l'atmosphère.
Il faut en outre déterminer la nature des autres constituants qui peuvent participer à un tel processus de dissociation. Un autre cas important est celui qui conduit à la production de l'oxyde d'azote, NO, à partir de l'hémioxyde d'azote N2O :

En fin de compte, il faut connaître l'abondance atmosphérique de ces constituants minoritaires comme H2O, N2O, etc.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Marcel NICOLET : professeur de géophysique externe à l'université de Bruxelles, professeur d'aéronomie, The Pennsylvania State University, États-Unis
Classification
Pour citer cet article
Marcel NICOLET. ATMOSPHÈRE - Chimie [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Article mis en ligne le et modifié le 10/02/2009
Médias
Autres références
-
ACCÉLÉROMÈTRES SPATIAUX
- Écrit par Raphaël F. GARCIA et Pierre TOUBOUL
- 4 883 mots
- 3 médias
...du sol à la frontière entre l'atmosphère et l'espace. En effet, comme le gradiomètre permet de mesurer les accélérations ressenties par le satellite, il est sensible aux variations de densité de l'air ainsi qu'aux déplacements des couches atmosphériques qui exercent une pression sur le satellite.... -
AÉRONOMIE
- Écrit par Gaston KOCKARTS
- 4 157 mots
- 11 médias
L' aéronomie a pour objet l'étude des régions atmosphériques où les phénomènes de dissociations moléculaires et d'ionisation sont importants. Cette définition s'applique aussi bien à l'atmosphère terrestre qu'aux atmosphères planétaires. Le mot aéronomie fut imaginé par Sidney Chapman (1888-1970) et...
-
AIR
- Écrit par Jean PERROTEY
- 2 154 mots
- 2 médias
Le globe terrestre est entouré d'une atmosphère constituée d'un mélange gazeux nommé air, qui s'étend de la surface du sol jusqu'à une altitude d'environ 150 kilomètres.
La pression de l'air au niveau de la mer a longtemps servi d'unité de pression (atmosphère) ; elle...
-
ANTARCTIQUE
- Écrit par Pierre CARRIÈRE , Edmond JOUVE , Jean JOUZEL , Gérard JUGIE et Claude LORIUS
- 16 481 mots
- 24 médias
...la circulation atmosphérique. Enfin, on a observé pour la première fois une corrélation directe entre l'évolution de la température et la teneur de l' atmosphère en gaz carbonique, les périodes les plus chaudes étant associées à des teneurs plus élevées et vice versa. En ce qui concerne l'époque récente,... - Afficher les 71 références






