- 1. Généralités
- 2. Atmosphère pure et sèche
- 3. Action des constituants minoritaires
- 4. Les constituants hydrogénés et la chimie mésosphérique
- 5. Les composés oxygénés de l'azote et la chimie stratosphérique
- 6. Les composés halogénés et la chimie stratosphérique
- 7. Les sources et les puits des composés hydrogénés, azotés et halogénés
- 8. Bibliographie
ATMOSPHÈRE Chimie
Atmosphère pure et sèche
On sait depuis plus d'un siècle que l'air pur et sec soumis à une décharge électrique produit de l'ozone par dissociation de l'oxygène. Dans l'atmosphère, le même phénomène apparaît sous l'effet du rayonnement ultraviolet solaire. On a successivement la photodissociation de O2 (coefficient J2), la reformation possible de O2 (coefficient k1) à haute altitude, au-delà de 70 km, la formation de l'ozone (coefficient k2), la photodissociation de O3 (coefficient J3) et, en fin de compte, la réaction entre O3 et O (coefficient k3) :
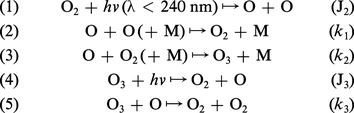
Dans ces équations, M est la troisième particule (N2 ou O2) donnant lieu à une collision triple requise pour capter l'énergie de dissociation de la molécule formée. Les conditions atmosphériques et les valeurs numériques attachées aux constantes de réaction et déterminées au laboratoire indiquent que le maximum de photodissociation de l'oxygène apparaît dans la stratosphère et conduit à un maximum de concentration de l'ozone également dans la stratosphère, à quelque 25 km d'altitude. Les études détaillées montrent que l'ozone est en équilibre photochimique dans le domaine atmosphérique situé au-dessus de son maximum de concentration. En d'autres termes, la production d'ozone sous l'effet de l'ultraviolet solaire est automatiquement compensée par la reformation de molécules d'oxygène.
On avait cependant déjà découvert, il y a plus d'un demi-siècle, que l'ozone ne se conformait pas aux variations du rayonnement solaire liées à la latitude ou à la saison. Ce comportement propre à l'ozone, avec maximum au printemps et minimum en automne et également avec une abondance supérieure aux hautes latitudes à celle des basses latitudes, a démontré que les réactions chimiques étaient lentes par rapport au transport atmosphérique dans la basse stratosphère, au-dessous de 25 km.
Ainsi, dans le cadre des études de chimie atmosphérique, il faut toujours associer les mouvements de l'atmosphère (transports verticaux et horizontaux) aux conditions qui régissent les réactions chimiques ne conduisant pas spontanément à l'équilibre photochimique. Si ces conditions s'appliquent à l'ozone dans la stratosphère inférieure, elles sont du même type pour l'atome d'oxygène dans la mésosphère supérieure, au-delà de 75 km. En effet, l'équation (3) indique que, par suite de la diminution de la concentration de O2 et de N2 quand l'altitude augmente, la formation de O3 devient de moins en moins importante. À partir de 60 km, la concentration de l'atome d'oxygène l'emporte sur celle de l'ozone. Néanmoins, cet atome est encore en équilibre photochimique jusqu'à 70 km, mais, au niveau de la mésopause (85 km), il est soumis aux mouvements atmosphériques et sa concentration locale dépend plus des conditions de transport que de celles de sa production.
Lorsqu'on effectue la comparaison des valeurs des concentrations théoriques et observées de l'ozone dans la stratosphère, on constate que les valeurs théoriques sont supérieures aux valeurs observées. Cette différence est due à l'effet de réactions qui n'apparaissent pas dans l'oxygène pur mais existent dans l'atmosphère réelle où de nombreux constituants minoritaires sont, en effet, présents.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Marcel NICOLET : professeur de géophysique externe à l'université de Bruxelles, professeur d'aéronomie, The Pennsylvania State University, États-Unis
Classification
Pour citer cet article
Marcel NICOLET. ATMOSPHÈRE - Chimie [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Article mis en ligne le et modifié le 10/02/2009
Médias
Autres références
-
ACCÉLÉROMÈTRES SPATIAUX
- Écrit par Raphaël F. GARCIA et Pierre TOUBOUL
- 4 883 mots
- 3 médias
...du sol à la frontière entre l'atmosphère et l'espace. En effet, comme le gradiomètre permet de mesurer les accélérations ressenties par le satellite, il est sensible aux variations de densité de l'air ainsi qu'aux déplacements des couches atmosphériques qui exercent une pression sur le satellite.... -
AÉRONOMIE
- Écrit par Gaston KOCKARTS
- 4 157 mots
- 11 médias
L' aéronomie a pour objet l'étude des régions atmosphériques où les phénomènes de dissociations moléculaires et d'ionisation sont importants. Cette définition s'applique aussi bien à l'atmosphère terrestre qu'aux atmosphères planétaires. Le mot aéronomie fut imaginé par Sidney Chapman (1888-1970) et...
-
AIR
- Écrit par Jean PERROTEY
- 2 154 mots
- 2 médias
Le globe terrestre est entouré d'une atmosphère constituée d'un mélange gazeux nommé air, qui s'étend de la surface du sol jusqu'à une altitude d'environ 150 kilomètres.
La pression de l'air au niveau de la mer a longtemps servi d'unité de pression (atmosphère) ; elle...
-
ANTARCTIQUE
- Écrit par Pierre CARRIÈRE , Edmond JOUVE , Jean JOUZEL , Gérard JUGIE et Claude LORIUS
- 16 481 mots
- 24 médias
...la circulation atmosphérique. Enfin, on a observé pour la première fois une corrélation directe entre l'évolution de la température et la teneur de l' atmosphère en gaz carbonique, les périodes les plus chaudes étant associées à des teneurs plus élevées et vice versa. En ce qui concerne l'époque récente,... - Afficher les 71 références






