SILICE
Le dioxyde de silicium ou silice occupe, parmi les oxydes, une place exceptionnelle ; en effet, par ses propriétés cristallochimiques, par ses modes de genèse, par son importance pétrographique, il s'apparente étroitement aux silicates. Dans la quasi-totalité de ses formes, il apparaît comme le modèle le plus simple des tectosilicates : une charpente tridimensionnelle faite de tétraèdres SiO4 liés les uns aux autres par leurs sommets, chaque atome d'oxygène étant commun à deux tétraèdres, d'où la formule globale SiO2. On connaît actuellement huit formes cristallisées de silice anhydre : le quartz, la tridymite, la cristobalite, la coésite, la kéatite, la stishovite, la mélanophlogite, la silice fibreuse W. À l'état amorphe, l'oxyde de silicium existe sous la forme de verre de silice anhydre et sous celle de silice colloïdale hydratée. La plupart de ces différentes silices – quartz, tridymite, cristobalite, coésite, stishovite, mélanophlogite, lechateliérite (verre de silice) et opales, silices hydratées plus ou moins amorphes – sont présentes dans la nature. Le quartz, et ses nombreuses variétés, est de très loin l'espèce la plus importante ; il est, avec les silicates qu'il accompagne fréquemment, l'un des minéraux majeurs de beaucoup de roches – en particulier des roches éruptives, dans la classification desquelles interviennent l'excès, la saturation ou le déficit en silice. Les nombreuses applications industrielles (optique, électronique, production de matériaux réfractaires, etc.) que connaît cette famille minérale accroissent encore l'intérêt des études qu'ont suscitées des propriétés et un rôle géochimique originaux.
Physico-chimie
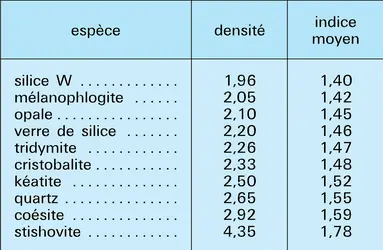
Il existe des relations étroites entre les structures des diverses silices. Toutes les formes sauf une, la stishovite, présentent les mêmes tétraèdres SiO4 s'associant par leurs sommets comme dans les tectosilicates (cf. silicates, fig. 1). Cependant, les modes d'association varient d'une espèce à l'autre, ce qui entraîne des différences dans les densités et les indices moyens de réfraction.
Transformations polymorphiques
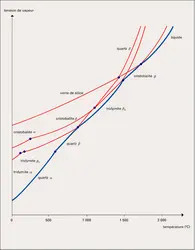
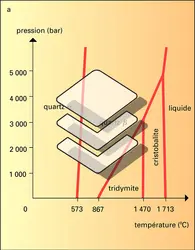
Les trois principales formes de silice – quartz, tridymite, cristobalite – correspondent chacune à des conditions d'équilibre bien définies. Leurs domaines de stabilité thermodynamique à la pression ordinaire ont été déterminés par C. N. Fenner en 1913. À la température ordinaire, le quartz, qui est stable, la tridymite et la cristobalite, qui sont métastables, sont des formes de basse température (dites B.T. ou α) ; elles subissent, quand on les chauffe, des transformations en formes de haute température (H.T. ou β) ; ces transformations, rapides et réversibles, sont appelées paramorphiques ou de déplacement, car elles comportent de faibles déplacements des atomes et de légères modifications des propriétés physiques, alors que les transformations mutuelles, dites non paramorphiques ou reconstructives, de ces trois formes de silice, dont les structures atomiques et les propriétés physiques diffèrent profondément, sont lentes, difficiles et nécessitent le plus souvent l'action d'un minéralisateur qui en augmente considérablement la vitesse. L'importance économique des minéralisateurs (sels alcalins ou alcalino-terreux principalement) peut être considérable, par exemple, dans l'industrie des réfractaires, où l'on utilise des briques de silice ; la matière première est le quartz sous la forme de grès ou de quartzites et des silex qu'il s'agit de transformer, au meilleur marché, en un mélange de tridymite et de cristobalite.
L'influence de la pression sur les transformations paramorphiques et non paramorphiques de la silice a été étudiée, en particulier, par H. S. Yoder (1950), O. F. Tuttle et N. L. Bowen (1958). La température de[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Maurice LELUBRE : professeur émérite à l'université de Toulouse-III-Paul-Sabatier
- Jean WYART : membre de l'Académie des sciences, professeur honoraire de l'université de Paris-VI-Pierre-et-Marie-Curie
Classification
Pour citer cet article
Maurice LELUBRE et Jean WYART. SILICE [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Médias
Autres références
-
ACIDES ROCHES
- Écrit par Jean-Paul CARRON
- 426 mots
En pétrographie, on qualifie de « roches acides » celles qui contiennent plus de 65 p. 100 en poids du constituant SiO2 (la silice). Comme les minéraux les plus siliceux — à l'exception bien entendu du quartz — sont les feldspaths alcalins, pour lesquels la teneur en SiO2 est précisément...
-
AGATE
- Écrit par Yves GAUTIER
- 710 mots
- 1 média
Dioxydes de silicium, les agates appartiennent au groupe des quartz microcristallins, comme les calcédoines et les jaspes. Elles se distinguent facilement des calcédoines car elles présentent une coloration zonée concentrique, sinueuse ou bréchique. Elles peuvent être cependant confondues avec l'onyx...
-
BÉTON
- Écrit par Jean-Michel TORRENTI
- 8 163 mots
- 1 média
-
CALCÉDOINE
- Écrit par Yves GAUTIER
- 793 mots
- 3 médias
- Afficher les 29 références
Voir aussi