OXYDES D'AZOTE
Articles
-
ATMOSPHÈRE - Chimie
- Écrit par Marcel NICOLET
- 3 553 mots
- 5 médias
L'importance des oxydes d'azote se manifeste par le cycle catalytique entre le monoxyde, NO, et le dioxyde, NO2 :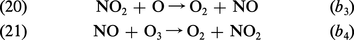
-
AUTOMOBILE - Défis
- Écrit par Daniel BALLERINI , François de CHARENTENAY , André DOUAUD , Francis GODARD , Gérard MAEDER et Jean-Jacques PAYAN
- 11 590 mots
- 8 médias
– des oxydes d'azote (NOx avec x = 1 ou 2) avec le monoxyde d'azote (NO) qui est formé en réponse aux hautes températures de combustion rencontrées dans le moteur ; NO peut s'oxyder en dioxyde d'azote (NO2) pendant la phase d'échappement et dans l'atmosphère. -
AZOTE
- Écrit par Encyclopædia Universalis et Paul HAGENMULLER
- 4 443 mots
- 4 médias
L' action de l'oxygène, qui mène au monoxyde d'azote NO, n'est possible qu'à température élevée, sous l'action d'un arc électrique par exemple. Même lorsque les produits de réaction sont soumis à une trempe brutale le rendement est encore très faible, NO étant endothermique à température ordinaire.... -
CARBURANTS
- Écrit par Daniel BALLERINI , Jean-Claude GUIBET et Xavier MONTAGNE
- 10 527 mots
- 9 médias
L'ozone est un polluant secondaire dans le sens où il se forme au cours de réactions chimiques complexes entre les hydrocarbures et les oxydes d'azote présents dans la basse couche de l'atmosphère (troposphère) et provenant, pour une part non négligeable, des rejets d'origine automobile. -
CYCLES BIOGÉOCHIMIQUES
- Écrit par Jean-Claude DUPLESSY
- 7 878 mots
- 6 médias
– Le peroxyde d'azote, NO2, gaz toxique irritant, déchet de l'industrie chimique, est produit dans l'atmosphère par oxydation de NO. -
ENVIRONNEMENT GLOBAL
- Écrit par Robert KANDEL
- 8 114 mots
- 10 médias
...compte dans les années 1960 que la faible quantité d'ozone dépendait aussi de cycles de destruction faisant intervenir d'autres molécules rares — des oxydes d'azote et d'hydrogène. Or la combustion des carburants dans les moteurs thermiques peut produire de tels oxydes. D'où une grande inquiétude sur... -
OZONE ATMOSPHÉRIQUE
- Écrit par Robert KANDEL
- 8 293 mots
- 6 médias
...l'ozone dans la stratosphère. D'autres processus doivent intervenir. Vers 1970, Paul Crutzen et Harold Johnston ont mis en évidence le rôle important des oxydes d'azote (généralement notés NOx), essentiellement le monoxyde d'azote ou oxyde nitrique (NO) et le dioxyde d'azote (NO2). Ces... -
POLLUTION
- Écrit par François RAMADE
- 20 869 mots
- 16 médias
Les oxydes d'azote, quoique toxiques pour les végétaux et les animaux à de fortes concentrations, constituent une catégorie importante d'aéropolluants, surtout à cause de leurs effets indirects. Ils se transforment en effet en des composés très dangereux, les peroxyacylnitrates (PAN) dans les atmosphères... -
POLLUTION ATMOSPHÉRIQUE URBAINE
- Écrit par Isabelle ROUSSEL
- 3 595 mots
- 4 médias
Lamesure des oxydes d’azote (NOX), polluants caractéristiques de la circulation automobile, s’est généralisée plus tardivement – seulement dans les années 1990 en France –, alors que l’augmentation du nombre de véhicules fut continue au cours du xxe siècle. Par exemple, à Paris... -
SULFURIQUE ACIDE
- Écrit par Gabriel TRIDOT
- 3 494 mots
- 3 médias
La fabrication de l'acide sulfurique utilise le procédé aux oxydes d'azote (procédé par chambres et par tours) ou le procédé de contact. Elle comprend deux phases successives : -
TUNNELS
- Écrit par Michel MAREC et Jean PÉRA
- 8 851 mots
- 6 médias
...pollué dans les tunnels de plus de 4 à 5 kilomètres de longueur, si les trains circulent dans les deux sens. Le polluant critique est constitué par les oxydes d'azote, mélange comportant environ 90 p. 100 de NO et 10 p. 100 de NO2. La teneur en oxyde d'azote, limite généralement admise, est de...
Média


