PYRIDINE
Formule brute : C5H5N
Masse moléculaire : 79,00 g
Point de solidification : — 42 0C
Point d'ébullition : 115,5 0C
Densité (à 0 0C) : 1,003
Liquide incolore d'odeur pénétrante caractéristique et désagréable, inflammable.
Ce composé hétérocycle aromatique possède un noyau qui présente une stabilité analogue à celle du noyau benzénique et qui fournit aussi trois isomères. Il n'y a pas de liaison azote-hydrogène.
Les bases dites pyridiques, homologues de la pyridine, ont été découvertes par Anderson (1846) dans les goudrons d'os ; on les rencontre aussi dans les goudrons de houille, de schiste et de lignite. La pyridine elle-même est miscible à l'eau, mais ses homologues supérieurs sont de moins en moins solubles, la solubilité étant plus grande à froid qu'à chaud, par suite de la formation d'hydrates stables à froid. Le noyau pyridique résiste à l'oxydation même sous l'action des oxydants les plus énergiques. Par réduction à l'aide de sodium et d'alcool, il conduit à des dérivés hexahydrogénés, les pipéridines.
On extrait la pyridine des goudrons d'os (huiles animales de Dippel) par action de l'acide sulfurique dilué. Après évaporation, on reprend par la soude et on distille.
La pyridine est largement utilisée comme solvant organique ; elle sert aussi à dénaturer l'éthanol commercial employé dans ce même but. Elle sert, en outre, à la fabrication de nombreux produits pharmaceutiques, à celle du caoutchouc et comme imperméabilisant, bactéricide et insecticide.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Bernard BACH : maître assistant à l'université de Nancy-I
Classification
Pour citer cet article
Bernard BACH. PYRIDINE [en ligne]. In Encyclopædia Universalis. Disponible sur : (consulté le )
Article mis en ligne le et modifié le 14/03/2009
Autres références
-
AROMATICITÉ
- Écrit par André JULG
- 4 706 mots
- 2 médias
De même, une molécule aromatique peut contenir des hétéroatomes. Par exemple, dans la pyridine C5H5N (formule 6), qui dérive formellement du benzène par le remplacement d'un groupement CH par un atome d'azote, c'est ce dernier qui fournit un électron au système conjugué. -
AZINES
- Écrit par Dina SURDIN
- 124 mots
Composés résultant de l'action des cétones ou des aldéhydes sur l'hydrazine.
Ils peuvent être soit en chaîne linéaire de formule générale R2C=N—N=CR2, soit cycliques dont la plus simple est la phénazine :
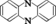
La phénazine et la phénazine N-substituée sont les deux produits de base...
-
HÉTÉROCYCLES
- Écrit par Jacques METZGER
- 4 695 mots
- 10 médias
Les cycles de base de cette série sont donnés dans la figure : pour l'hétéroatome azote, la pyridine, les dihydropyridines et, notamment, les pyridones, la pipéridine ; pour l'hétéro-atome oxygène ou soufre, les 2H-pyranne et thiopyranne et les 4H-pyranne et thiopyranne et, notamment, les pyrones,... -
PIPÉRIDINE
- Écrit par Dina SURDIN
- 171 mots
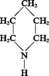
Masse moléculaire : 85,15 g
Masse volumique : 0,8622 g/cm3.
Point de fusion : — 7 0C (solidification de — 13 à — 17 0C)
Point d'ébullition : + 106,5 0C
Liquide incolore, d'odeur caractéristique, savonneux au toucher. Miscible à l'eau, l'alcool, l'éther ; soluble dans le...


