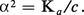OSTWALD LOI DE DILUTION D'
Articles
-
ACIDES & BASES
- Écrit par Yves GAUTIER, Pierre SOUCHAY
- 12 364 mots
- 7 médias
...au nombre total de molécules ; si α est voisin de 1, on dit que l'acide ou la base est fort (HCl, KOH) ; s'il est faible, on dit que l'électrolyte est faible (acide acétique, ammoniaque NH4OH).Pour un acide ou une base de concentration globale C, il existe entre α et K la relation d'Ostwald :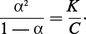
-
ÉLECTROCHIMIE
- Écrit par Jacques SIMONET
- 6 252 mots
- 10 médias
Cette théorie, due à Svante Arrhenius, permet de distinguer les électrolytes « forts » et « faibles » selon que α est supérieur ou inférieur à 0,1. Elle permet d'expliquer l'effet de la dilution sur la conductivité (loi d'Ostwald). -
THERMODYNAMIQUE - Thermodynamique chimique
- Écrit par Pierre SOUCHAY
- 7 192 mots
- 3 médias
...fraction dissociée comprise entre 0 et 1 ; les concentrations de A- et de B+ sont chacune égales à αc, et celle de AB non dissocié est pratiquement égale à c si l'on admet que α est faible. La loi d'action de masse appliquée aux concentrations donne la loi de dilution d'Ostwald :