HYDROXYLE ou OXHYDRYLE
Articles
-
ACIDES & BASES
- Écrit par Yves GAUTIER, Pierre SOUCHAY
- 12 364 mots
- 7 médias
...et bases, elle permit de préciser les notions précédentes et de les rendre quantitatives. Un acide HA est une substance qui, en solution aqueuse, fournit, lors de son équilibre de dissociation, des protons H+ :une base BOH est une substance qui, dans les mêmes conditions, fournit desions OH—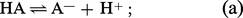
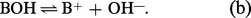
-
ALCOOLS
- Écrit par Jacques METZGER
- 5 832 mots
- 8 médias
Le mot alcool, de l'arabe al khoul ou al koh'l, désignait à l'origine une poudre très fine à base de stibine (sulfure d'antimoine). À ce mot s'attacha une idée de finesse et de subtilité, de sorte que les alchimistes l'appliquaient aussi bien à des poudres impalpables résultant d'une sublimation...
-
CATALYSE
- Écrit par Henri Jean-Marie DOU, Jean-Eugène GERMAIN
- 8 394 mots
- 7 médias
...plus ancienne réaction de catalyse par les bases est la saponification des matières grasses, c'est-à-dire la manufacture du savon. Le vrai catalyseur est l'ion hydroxyle OH—(soude ou potasse dans l'eau), qui se combine à la fonction ester en un intermédiaire d'où s'élimine un ion alcoxyle OR... -
HYDROXYDES
- Écrit par Bertrand DREYFUS
- 182 mots
Composés chimiques contenant un ou plusieurs groupes d'ions hydroxyles (OH—). Le cation est en général un ion métallique (Na, K, Mg, Ca, Al) ou un radical organique (comme le tétraméthylammonium).
Les hydroxydes sont des bases plus ou moins fortes, les plus fortes étant celles des métaux...
-
LIAISONS CHIMIQUES - Liaison hydrogène
- Écrit par André JULG
- 3 328 mots
- 2 médias
Les propriétés chimiques des composés possédant des groupements OH mettent en évidence l'existence d'associations entre les molécules par l'intermédiaire de ces groupements. L'énergie de ces associations est en général beaucoup plus faible que les énergies rencontrées pour les liaisons entre les...
-
MÉTHANE ET CLIMAT
- Écrit par Hervé HERBIN
- 4 692 mots
- 4 médias
Le principal puits de méthane est dû aux réactions d’oxydation de cette molécule avec le radical hydroxyle (OH) au sein de la troposphère (permettant l’élimination de 450 à 550 Mt de méthane par an) et de la stratosphère (de 10 à 50 Mt par an) pour former de l’eau et du dioxyde de carbone. Plus... -
PHÉNOLS
- Écrit par Jacques METZGER
- 3 352 mots
- 2 médias
Les acides les plus forts sont incapables, dans le cas des phénols simples, de remplacerl'hydroxyle par un autre anion ; cependant, cette substitution devient facile si le phénol porte en ortho- et en para- des groupes accepteurs forts comme −NO2 (préparation du chlorure de picryle à partir...


