BASE, chimie
Articles
-
ACIDES & BASES
- Écrit par Yves GAUTIER, Pierre SOUCHAY
- 12 364 mots
- 7 médias
-
ALDOLS & CÉTOLS
- Écrit par Jacques METZGER
- 1 406 mots
- 3 médias
Les β-aldols résultent de l'action, sur les aldéhydes énolisables, de bases moyennement fortes comme KCN, Na2CO3 ou NaOH diluée :L'ensemble des réactions est réversible et l'équilibre est largement déplacé vers la formation de l'aldol. Cette aldolisation peut être également catalysée par les acides...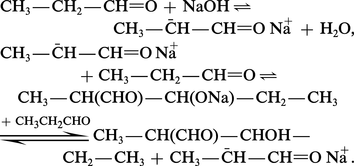
-
AMINES
- Écrit par Jacques METZGER
- 3 232 mots
- 4 médias
Basicité. Les amines des trois classes sont des bases de Lewis : elles forment, avec les acides, des adduits dans une réaction équilibrée. Vis-à-vis du proton et en phase gazeuse, c'est-à-dire en l'absence de solvatation des ions, la réaction :conduit à un ordre de basicité croissante...
-
AMMONIAC
- Écrit par Henri GUÉRIN
- 5 033 mots
- 5 médias
En milieu aqueux, l'ammoniac est donc une base au sens d'Arrhenius, puisqu'il y a libération d'ions hydroxyles. Il s'agit en fait d'une base faible caractérisée par une constante de dissociation très faible (Kb = 1,85 ( 10—5, ou pKb = 4,73) : dans une solution décimolaire,... -
AMMONIUM ION
- Écrit par Dina SURDIN
- 74 mots
L'ion ammonium, NH+4, présente des propriétés basiques et peut être comparé aux ions des métaux alcalins. L'ion ammonium se combine à l'oxhydrile OH— pour donner l'ammoniaque NH4OH.
Le chlorure d'ammonium, NH4Cl, est employé dans les piles sèches comme électrolyte....
-
AZOTE
- Écrit par Universalis, Paul HAGENMULLER
- 4 443 mots
- 4 médias
Par suite de son caractère donneur, N2H4 possède des propriétés basiques en solution aqueuse :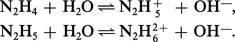
-
CATALYSE
- Écrit par Henri Jean-Marie DOU, Jean-Eugène GERMAIN
- 8 394 mots
- 7 médias
Laplus ancienne réaction de catalyse par les bases est la saponification des matières grasses, c'est-à-dire la manufacture du savon. Le vrai catalyseur est l'ion hydroxyle OH—(soude ou potasse dans l'eau), qui se combine à la fonction ester en un intermédiaire d'où s'élimine un ion... -
COORDINATION (chimie) - Composés de coordination
- Écrit par Jean AMIEL, Jean-Pierre SCHARFF
- 4 894 mots
- 4 médias
Ce type de notion a été développé par Pearson (1963) dans la théorie des acides (ions métalliques) durs et mous et desbases (coordinats) dures et molles. C'est la théorie H.S.A.B. (hard and soft acid base theory). La classification correspondante présente de grandes analogies avec la... -
ÉTHERS-OXYDES
- Écrit par Jacques METZGER
- 1 967 mots
- 1 média
Leurs propriétés basiques (pKa = − 3,5) se manifestent dans la formation de complexes (adduits) divers : le dioxane forme avec le brome un composé d'addition, le dibromure de dioxane, bien cristallisé, utilisé comme agent de bromation. -
HÉTÉROCYCLES
- Écrit par Jacques METZGER
- 4 695 mots
- 10 médias
Une méthode générale (réaction) consiste àtraiter par une base un dérivé difonctionnel-1,2 dans lequel l'une des fonctions, nucléophile, apporte l'hétéroatome Z (amine Z = NH, alcool Z = O, thiol Z = S) et l'autre, Y, est un groupe facilement remplaçable par un mécanisme SN... -
PYRIDIQUES BASES
- Écrit par Dina SURDIN
- 188 mots
Homologues de la pyridine ; on connaît les picolines, ou méthylpyridines, de formule brute C6H7N ; les lutidines, de formule brute C7H9N (diméthylpyridines et éthylpyridines) ; les collidines, de formule brute C8H11N (triméthylpyridines, propylpyridines, méthyléthylpyridines).
L'α-picoline...
Média



