ÉLÉMENTS CHIMIQUES
Articles
-
ASTRONOMIE
- Écrit par James LEQUEUX
- 11 339 mots
- 20 médias
...En 1860, Gustav Kirchhoff (1824-1887) et Robert Bunsen (1811-1899) reconnaissent dans la lumière du Soleil les traits caractéristiques de plusieurs éléments chimiques. Grâce aux progrès de la spectroscopie, Henry Rowland (1848-1901) dénombrera trente-six de ces éléments en 1896. Joseph Norman Lockyer... -
ATOME
- Écrit par José LEITE LOPES
- 9 140 mots
- 13 médias
L'atome est le terme ultime de la division de la matière dans lequel les éléments chimiques conservent leur individualité. C'est la plus petite particule d'un élément qui existe à l'état libre ou combiné. On connaît 90 éléments naturels auxquels s'ajoutent le ...
-
ATOMIQUE PHYSIQUE
- Écrit par Philippe BOUYER, Georges LÉVI
- 6 651 mots
- 1 média
Les énergies εn,l dépendent relativement peu du choix du champ central, ce qui a permis d'établir une classification périodique des éléments. Si l'on ne considère, pour simplifier, que l'énergie la plus faible possible (énergie du niveau fondamental) d'un atome neutre, les ... -
ATOMIQUE THÉORIE
- Écrit par Pierre LASZLO
- 1 434 mots
La deuxième conjecture est l'indiscernabilité de ces corpuscules. Les atomes d'un même élément sont tous identiques, mais les éléments se distinguent les uns des autres par des atomes différents. Les atomes de fer, par exemple, diffèrent de ceux de cuivre. -
BERZELIUS JÖNS JACOB (1779-1848)
- Écrit par Jacques GUILLERME
- 2 014 mots
- 1 média
...d'innombrables analyses comparatives et exprima dans un système de notations simples les équivalences pondérales, qu'il développa entre 1811 et 1818. Chaque élément y est noté par une ou deux lettres ; encore en usage pour la plupart, ces signes n'étaient pas de simples repérages sténographiques, mais... -
BIG BANG
- Écrit par Marc LACHIÈZE-REY
- 2 533 mots
- 4 médias
...primordiale. Dans les années 1930, le physicien d'origine russe George Gamow (1904-1968), qui séjourne alors à Göttingen, en Allemagne, est intrigué par l'uniformité de la distribution des éléments chimiques, sur Terre, et dans l'Univers. Il émet d'abord l'idée que tous ces éléments ont pu être fabriqués... -
BIOSPHÈRE
- Écrit par Paul DUVIGNEAUD, Maxime LAMOTTE, François RAMADE
- 3 431 mots
- 5 médias
Les éléments chimiques qui sont présents dans la biosphère, c'est-à-dire qui constituent la matière des êtres vivants, sont nombreux, mais leur importance quantitative est très variable. Le carbone est l'élément de base de la matière organique, qui renferme aussi en quantités non négligeables de l'azote,... -
BOHR NIELS (1885-1962)
- Écrit par Léon ROSENFELD
- 3 114 mots
- 1 média
...molécules polyatomiques (ces dernières comportant plusieurs noyaux). Ainsi, Bohr suggérait l'identification du numéro atomique, indiquant la place d'un élément dans le tableau périodique, avec le nombre des électrons périphériques, plus fondamental que la masse atomique des chimistes ; il en tirait même,... -
CHIMIE - Histoire
- Écrit par Élisabeth GORDON, Jacques GUILLERME, Raymond MAUREL
- 11 186 mots
- 7 médias
Il faut peut-être attendre Jungius, puis, surtout, en 1664, le Sceptical Chymist de Boyle pour trouver unedéfinition générique satisfaisante de l'élément, rapportée à une nécessaire rationalité instrumentale. Boyle attribue justement la qualité élémentaire à tout corps indécomposable. C'est la technique... -
CHIMIE - La chimie aujourd'hui
- Écrit par Pierre LASZLO
- 10 856 mots
- 3 médias
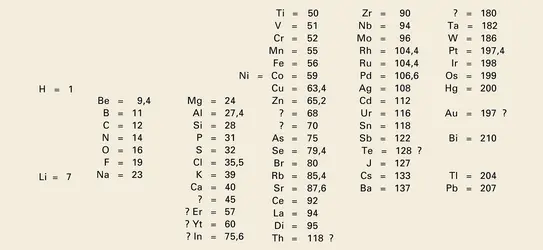
Étude des éléments et de leurs propriétés influencées par la structure du noyau de l'atome, elle se partage entre l'exploration et les applications. La première s'illustre par la formation d'éléments artificiels, qui viennent prolonger le système périodique des éléments (ou tableau de Mendeleïev).... -
CHIMIE - La nomenclature chimique
- Écrit par Nicole J. MOREAU
- 5 031 mots
- 7 médias
Leséléments portent des noms, qui sont triviaux et datent de leur découverte ; certains sont très anciens et dérivent du latin, alors que d'autres sont plus modernes. Pour les noms anciens, la dénomination est souvent différente dans les diverses langues, pour conserver un nom en usage depuis longtemps... -
COSMOLOGIE
- Écrit par Marc LACHIÈZE-REY
- 9 300 mots
- 6 médias
...essentiellement des neutrons, des protons et des électrons pour la matière, des photons et des neutrinos pour le rayonnement. Il n'existe donc aucun noyau d'élément chimique puisque ceux-ci sont des assemblages liés de nucléons (sauf bien entendu des noyaux d'hydrogène, qui se réduisent à un seul proton).... -
CYCLES BIOGÉOCHIMIQUES
- Écrit par Jean-Claude DUPLESSY
- 7 878 mots
- 6 médias
L'activité de la Terre est incessante : toutes ses couches – du noyau à la plus haute atmosphère – sont animées de continuels mouvements et, surtout, ses enveloppes superficielles – l'atmosphère, les océans et la surface des continents – abritent la vie. Les atomes et les molécules qui constituent...
-
ÉCLAIRAGE DOMESTIQUE
- Écrit par Georges ZISSIS
- 8 154 mots
- 12 médias
...protéger le filament, la lampe halogène renferme également un gaz halogéné – qui se présente dans ce cas sous la forme d’un composant organique du brome, élément chimique de la famille des halogènes. Ce gaz permet d’augmenter la température du filament de tungstène (donc le rendement de la lampe) sans détériorer... -
ÉLÉMENTS NATIFS
- Écrit par Guy ROGER
- 2 071 mots
- 3 médias
Un élément est dit « natif » lorsqu'il se trouve à l'état de corps simple, non combiné à d'autres éléments. Les gaz rares (hélium, néon, argon, krypton, xénon, radon), chimiquement inertes, n'entrent dans aucune combinaison et sont donc toujours à l'état natif. Dans la croûte...
-
FOWLER WILLIAM (1911-1995)
- Écrit par Bernard PIRE
- 743 mots
L’astrophysicien américain William Fowler a consacré sa vie, au sein du laboratoire Kellogg de physique nucléaire de l'Institut de technologie de Californie (Caltech) à Pasadena, à comprendre comment les différents éléments chimiques ont pu se former dans l'Univers. Il est considéré...
-
GAZ RARES ou GAZ NOBLES
- Écrit par Paul ALLAMAGNY, Universalis, Albert LACAZE, Nathalie LEMAITRE
- 3 902 mots
- 2 médias
L'hélium, le néon, l'argon, le krypton, le xénon et le radon forment la famille des gaz rares, groupe zéro de la classification périodique des éléments chimiques. Tous monoatomiques, ces gaz sont caractérisés par leur très grande inertie chimique, d'où les qualificatifs de nobles ou d'inertes...
-
GÉOCHIMIE
- Écrit par Marie-Laure PONS
- 2 062 mots
- 4 médias
La géochimie est une science qui applique les principes de la chimie à l'explication des processus géologiques, passés et présents, qui affectent les enveloppes terrestres internes (noyau, manteau, croûtes) et externes (océans, atmosphère, biosphère). Le Glossary of Geology and Related...
-
HALOGÈNES
- Écrit par Jacques METZGER, Robert de PAPE
- 6 600 mots
- 5 médias
-
HYDROGÈNE (physique)
- Écrit par Bernard PIRE
- 6 157 mots
- 9 médias
L’hydrogène est l’élément le plus répandu dans l’Univers. Au début du xviie siècle, l’alchimiste genevois Turquet de Mayerne (1573-1655), poursuivant une observation de Paracelse (1493-1541), observe un dégagement de gaz lorsqu’un acide (esprit de vitriol) agit sur du fer ou du zinc. Le...
- 1
- 2
Médias